钛和钛的合金已被广泛用于制造电讯器材 人造骨骼 化工设备 飞机等航天航空材料 被誉为“未来世界的金属
| 钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”。试回答下列问题: (1)钛有 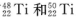 两种原子,它们互称为____。元素在元素周期表中的位置是第_____周期,第____族;基态原子的电子排布式为_____;按电子排布Ti元素在元素周期表分区中属于_____区元素。 两种原子,它们互称为____。元素在元素周期表中的位置是第_____周期,第____族;基态原子的电子排布式为_____;按电子排布Ti元素在元素周期表分区中属于_____区元素。(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构如图所示,它的化学式是______, 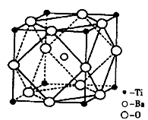 (3)氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金装饰的替代品。以TiCl4为原料,经过一系列反应,可以制Ti3N4和纳米TiO2  。 。①Ti3N4中元素的化合价为_____。TiCl4分子中4个氯原子不在同一平面上,则TiCl4的空间构型为______。 ②反应①为置换反应、该反应的化学方程式为______。 ③纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如下: 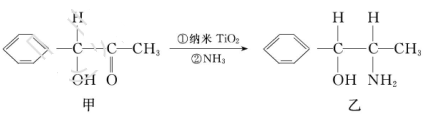 化合物甲的分子中采取 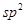 杂化的碳原子个数为_____,化合物乙中采取 杂化的碳原子个数为_____,化合物乙中采取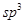 杂化的原子的第一电离能由大到小的顺序为_____。 杂化的原子的第一电离能由大到小的顺序为_____。④有一种氮化钛晶体的晶胞如图所示,该氮化钛晶胞中含有______个N原子,晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为______g. 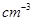 (NA为阿伏加德罗常数的数值,只列算式)。 (NA为阿伏加德罗常数的数值,只列算式)。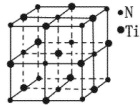 |
参考解答
| (1)同位素 四 IVB 1s22s22p63s23p63d24s2 d; (2)BaTiO3 (3)①+4 正四面体;② 2Mg+TiCl4  Ti+2MgCl2 ③7 N>O>C ;④4 Ti+2MgCl2 ③7 N>O>C ;④4 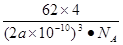 |
试题分析:(1)钛的这两种原子质子数相同,而中子数不同,使用属于同位素。22元素Ti在元素周期表中的位置是第四周期第ⅣB。基态Ti原子的电子排布式为1s22s22p63s23p63d24s2。按电子排布Ti元素在元素周期表分区中属于d区元素。(2)在每个偏钛酸钡晶体中晶胞中含有Ba:1;Ti:8×1/8='1;' O:12×1/4=3.所以偏钛酸钡的化学式是BaTiO3. (3)①根据在任何化合物中正负化合价的代数和为0的原则。可知:在Ti3N4中元素的化合价为Ti:+4价,N:-3价。由于在TiCl4中四个Cl原子不在一个平面内。则TiCl4的空间构型为 正四面体型。②TiCl4与Mg发生的是为置换反应,该反应的化学方程式为Mg+TiCl4  Ti+2MgCl2。③在化合物 Ti+2MgCl2。③在化合物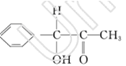 中采用sp2杂化的碳原子有苯环上的6个C原子和羰基 中采用sp2杂化的碳原子有苯环上的6个C原子和羰基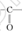 上的C原子,共有7个C原子。化合物乙 上的C原子,共有7个C原子。化合物乙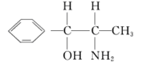 中采取 中采取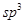 杂化的原子有C、N、O三个,当原子核外的电子处于全充满、半充满或全空时是稳定的状态,N原子的2p轨道处于半充满的稳定状态。其余的则原子核外的电子数越多,原子越难失去电子。因此它们的第一电离能由大到小的顺序为N>O>C。④N原子在顶点和面心上,Ti在棱边上和体内。所以每个晶胞中含有的原子个数为:N:8×1/8+6×1/2=4;Ti:12×1/4+1=4.即每个晶胞内含有4个TiN。由晶胞图可知:晶胞的边长为2a×10-10cm. 杂化的原子有C、N、O三个,当原子核外的电子处于全充满、半充满或全空时是稳定的状态,N原子的2p轨道处于半充满的稳定状态。其余的则原子核外的电子数越多,原子越难失去电子。因此它们的第一电离能由大到小的顺序为N>O>C。④N原子在顶点和面心上,Ti在棱边上和体内。所以每个晶胞中含有的原子个数为:N:8×1/8+6×1/2=4;Ti:12×1/4+1=4.即每个晶胞内含有4个TiN。由晶胞图可知:晶胞的边长为2a×10-10cm.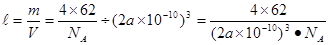 |
相似问题
用Cr3+掺杂的氮化铝是理想的LED用荧光粉基质材料 氮化铝(其晶胞如图所示)可由氯化铝与氨经气相反
用Cr3+掺杂的氮化铝是理想的LED用荧光粉基质材料,氮化铝(其晶胞如图所示)可由氯化铝与氨经气相反应制得。(1)Cr3+基态的核外电子排布式可表示为。(2
铜 铁 钒都是日常生活中常见的金属 具有广泛用途。请回答:(1)在元素周期表中 铜元素位于____区
铜、铁、钒都是日常生活中常见的金属,具有广泛用途。请回答:(1)在元素周期表中,铜元素位于____区,其基态原子的电子排布式为。(2)Cu2O的熔点比Cu2
已知周期表中 元素Q R W Y与元素X相邻。Y的最高化台价氧化物的水化物是强酸。回答下列问题: (
已知周期表中,元素Q、R、W、Y与元素X相邻。Y的最高化台价氧化物的水化物是强酸。回答下列问题: (1)W与Q可以形成一种高温结构陶瓷材料。W的氯化物分
已知A B C D E F G为前四周期七种元素且原子序数依次增大 其中A的基态原子中没有成对电子;
已知A、B、C、D、E、F、G为前四周期七种元素且原子序数依次增大,其中A的基态原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种
[物质结构与性质]已知:A B C D E F六种元素 原子序数依次增大。A原子核外有两种形状的电子
[物质结构与性质]已知:A、B、C、D、E、F六种元素,原子序数依次增大。A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等;B是短周期中原












