已知A B C D E F G为前四周期七种元素且原子序数依次增大 其中A的基态原子中没有成对电子;
| 已知A、B、C、D、E、F、G为前四周期七种元素且原子序数依次增大,其中A的基态原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,C原子核外成对电子数比未成对电子数多1个,其氢化物常用作致冷剂,D原子未成对电子与周期数相同,在E元素所在周期中的基态该原子的第一电离能最小;F原子价电子nsn-lnpn+l;G单质是硬度最大的金属。 请回答下列问题: (1)G元素基态原子价电子排布式为 。 (2)B、C、D三种元素的最简单氢化物的键角由小到大的顺序为____ (填元素符号),常温下硬度最大的B单质、E2F、H2D及H2F的沸点由大到小的顺序为____ (填化学式) (3)D元素与氟元素相比,电负性:D 氟元素(填“>”、“=”或“<”), 下列表述中能证明这一事实的是 (填选项序号)- A.常温下氟气的颜色比D单质的颜色深 B.氟气与D的氢化物剧烈反应,产生D的单质 C.氟与D形成的化合物中D元素呈正价态 D.比较两元素的单质与氢气化合时得电子的数目 (4)离子化合物CA5的晶体中含有多种化学键:但一定不含有的化学键是 (填选项序号)。 A.极性键 B.非极性键 C.配位键 D.金属键 (5)B2A4是重要的基本石油化工原料。B2A4分子中B原子轨道的杂化类型为____ ;1molB2A4分子中含 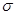 键 mol。 键 mol。(6)如图是E的氯化物的晶胞示意图,最近两个E离子之间距离为a cm,则该晶体密度为 (已知阿伏加德罗常数为NA). 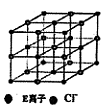 |
参考解答
| (1)3d54s1 (2)O、N、C C、Na2S 、H2O、 H2S (3)< B、C (4)B、D (5)sp2杂化 ; 5 (6) 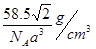 |
试题分析:根据题意可推出这几种元素分别是:A是H;B是C;C是N;D是O;E是Na;F是S;G 是Cr。(1)Cr元素基态原子价电子排布式为 3d54s1 。2)甲烷的键角为109°28′;NH3的键角为键角为107°18′;H2O的键角为104.3°。所以它们键角由小到大的顺序为O、N、C。常温下硬度最大的C单质金刚石属于原子晶体;Na2S属于离子晶体;H2O及H2S都属于分子晶体。一般情况下沸点的高低顺序是:原子晶体>离子晶体>分子晶体。由于在H2O之间存在氢键,增加了分子之间的相互作用,所以沸点H2O>H2S。故沸点由大到小的顺序为C> Na2S > H2O > H2S 。(3)元素的非金属性越强,其电负性就越大。由于非金属性F>O。所以电负性F>O。(4)离子化合物NH5可表示为NH4H.在其晶体中含有的化学键包括离子键、极性共价键、配位键。不含有非极性键和金属键。因此选项为B、D。(5)在C2H4中C原子轨道的杂化类型为sp2杂化。1mol C2H4分子中含 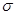 键有4和C—H键和一个C—C键共5个。(6)在每个晶胞中含有的Na+个数为:8×1/8+6×1/2=4;含有的Cl-的个数为:12×1/4+1=4。即每个晶胞中含有4个NaCl。最近两个Na+在面对角线的位置的一半,设晶胞的边长为L.其离子之间距离为a cm。 键有4和C—H键和一个C—C键共5个。(6)在每个晶胞中含有的Na+个数为:8×1/8+6×1/2=4;含有的Cl-的个数为:12×1/4+1=4。即每个晶胞中含有4个NaCl。最近两个Na+在面对角线的位置的一半,设晶胞的边长为L.其离子之间距离为a cm。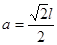 。所以 。所以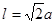 。该晶体密度为 。该晶体密度为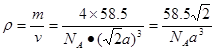 g/cm3. g/cm3. |
相似问题
[物质结构与性质]已知:A B C D E F六种元素 原子序数依次增大。A原子核外有两种形状的电子
[物质结构与性质]已知:A、B、C、D、E、F六种元素,原子序数依次增大。A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等;B是短周期中原
已知A B C D E五种元素的原子序数依次增大 其中A原子所处的周期数 族序数都与其原子序数相等;
已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态;D原子L电子层上有2
下表为长式周期表的一部分 其中的编号代表对应的元素。(1)元素③基态原子的电子排布式为
下表为长式周期表的一部分,其中的编号代表对应的元素。(1)元素③基态原子的电子排布式为。(2)②与⑦形成的化合物的空间构型为。(3)元素②④⑤⑥的
粉煤灰是燃煤电厂的工业废渣 其中含莫来石(Al6Si2O13)的质量分数为38% 还有含量较多的Si
粉煤灰是燃煤电厂的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为38%,还有含量较多的SiO2。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4,有关化学反
现有aA bB cC dD eE gG六种短周期元素 a+b=c a+c=d a+d=e d+e=g
现有aA、bB、cC、dD、eE、gG六种短周期元素,a+b=c,a+c=d,a+d=e,d+e=g,B、C、E、G的单质均有多种同素异形体,请回答下列问题:Ⅰ.(1)C、D、E元素












