已知A B C D E五种元素的原子序数依次增大 其中A原子所处的周期数 族序数都与其原子序数相等;
| 已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态;D原子L电子层上有2对成对电子;E+原子核外有3层电子且各层均处于全满状态。 请填写下列空白。 (1)E元素基态原子的核外电子排布式为 。 (2)B、C、D三种元素的第一电离能数值由小到大的顺序为 (填元素符号),其原因为 。 (3)B2A4是重要的基本石油化工原料。B2A4分子中B原子轨道的杂化类型为 ;1 mol B2A4分子中含 mol σ键。 (4)已知D、E能形成晶胞如下图所示的两种化合物,化合物的化学式,甲为 ,乙为 ;高温时,甲易转化为乙的原因为 。 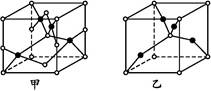 |
参考解答
| (1)1s22s22p63s23p63d104s1 (2)C<O<N 同一周期,随着原子序数的增加,元素的第一电离能呈现逐渐增大的趋势,但氮元素的最外层电子达到半充满的稳定构型,其第一电离能大于氧元素 (3)sp2 5 (4)CuO Cu2O Cu2O中Cu的d轨道为全充满状态,较稳定 |
A为H;B原子核外有6个电子,为碳;由2p2、2p4,且B原子为碳原子,可知D只能为O原子,C只能为N原子;E+的核外电子排布式为1s22s22p63s23p63d10,可知E为Cu;(3)由CH2 CH2可知一个乙烯分子中含有5个σ键;(4)甲中小黑点为4个,小白点8个顶点、4个棱、2个面心、1个体心,共4个;乙中小黑点为4个,小白点8个顶点、1个体心,共2个;所以甲表示CuO、乙表示Cu2O;找出CuO、Cu2O的不同点,铜的价态不同,从核外电子排布式分析即可 CH2可知一个乙烯分子中含有5个σ键;(4)甲中小黑点为4个,小白点8个顶点、4个棱、2个面心、1个体心,共4个;乙中小黑点为4个,小白点8个顶点、1个体心,共2个;所以甲表示CuO、乙表示Cu2O;找出CuO、Cu2O的不同点,铜的价态不同,从核外电子排布式分析即可 |
相似问题
下表为长式周期表的一部分 其中的编号代表对应的元素。(1)元素③基态原子的电子排布式为
下表为长式周期表的一部分,其中的编号代表对应的元素。(1)元素③基态原子的电子排布式为。(2)②与⑦形成的化合物的空间构型为。(3)元素②④⑤⑥的
粉煤灰是燃煤电厂的工业废渣 其中含莫来石(Al6Si2O13)的质量分数为38% 还有含量较多的Si
粉煤灰是燃煤电厂的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为38%,还有含量较多的SiO2。用粉煤灰和纯碱在高温下烧结,可制取NaAlSiO4,有关化学反
现有aA bB cC dD eE gG六种短周期元素 a+b=c a+c=d a+d=e d+e=g
现有aA、bB、cC、dD、eE、gG六种短周期元素,a+b=c,a+c=d,a+d=e,d+e=g,B、C、E、G的单质均有多种同素异形体,请回答下列问题:Ⅰ.(1)C、D、E元素
下列关于化合价的判断正确的是 [ ]A.Na2O中O元素为-1价
下列关于化合价的判断正确的是 [ ]A Na2O中O元素为-1价B Na2O2中O元素为-2价 C SO2中O元素为-1价D SO3中O元素为-2价
下列各组物质各自形成的晶体 均属于分子晶体的化合物的是( )。A.NH3 HD C10H8
下列各组物质各自形成的晶体,均属于分子晶体的化合物的是()。A.NH3、HD、C10H8B.PCl3、CO2、H2SO4C.SO2、SiO2、P2O5D.CCl4、Na2S、H2O2












