现有aA bB cC dD eE gG六种短周期元素 a+b=c a+c=d a+d=e d+e=g
| 现有aA、bB、cC、dD、eE、gG六种短周期元素,a+b=c,a+c=d,a+d=e,d+e=g,B、C、E、G的单质均有多种同素异形体,请回答下列问题: Ⅰ.(1)C、D、E元素的第一电离能由大到小的关系为____________。(用相应的元素符号表示) (2)请比较C2A4、D2A4、G2A4三种化合物的沸点由高到低的顺序为 ____________________。(用化学式表示) (3)有某种分子式为C4D4E8的物质(该物质中同种原子的化学环境完全相同,不含碳碳双键)是一种威力极强的炸药,则可推知其结构简式为____________。 Ⅱ.BG是一种耐磨材料,其与金刚石结构相似,右图为其结构中的最小重复单元,它可由B的三溴化物和G的三溴化物于高温下在氢气的氛围中合成。 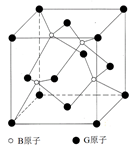 (1)指出B的三溴化物中B的杂化方式为___________;G的三溴化物分子的结构为_________型。 (2)写出合成BG的化学反应方程式为_______________________________。 (3)已知晶体中B与G原子的最近距离为a pm,则该晶体的密度的表达式为__________g/cm3。(不需化简) |
参考解答
| Ⅰ.(1)N>O>C (2分) (2)N2H4>P2H4>C2H4 (2分) (3) 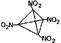 (2分) (2分)Ⅱ.(1)sP2 (2分);三角锥 (1分)。 (2)BBr3+PBr3+3H2 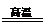  BP+6HBr (3分) BP+6HBr (3分)(3) 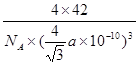 (3分) (3分) |
试题分析:由a+b=c,a+c=d,a+d=e,知b、c、d、e间相差a,在短周期内,猜想a=1,且B、C、E、G的单质均有多种同素异形体,则b、c、d、e分别等于5、6、7、8,g=15,对应元素分别是H、B、C、N、O、P,B、C、O、P均有同素异形体。 Ⅰ.(1)N的最外层为半充满状态,第一电离能最大,C、O则按照同周期元素第一电离能的比较即可,则C、N、O的第一电离能由大到小的关系为N>O>C (2)C2A4、D2A4、G2A4三种化合物的化学式为C2H4、N2H4、P2H4,它们均属于分子晶体,但N2H4分子间存在氢键,所以沸点最高,其他两种符合相对分子量越大,分子间作用力越大,沸点越高,所以沸点的高低顺序是N2H4>P2H4>C2H4 (3)分子式为C4D4E8的物质的最简式为CNO2, 该物质中同种原子的化学环境完全相同,不含碳碳双键,所以每个碳原子与其他3个碳原子相连,同时与一个硝基相连,其结构简式为 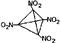 Ⅱ.(1)B的三溴化物的化学式为BBr3,中心原子的价层电子对数是3,所以是sp2杂化,G的三溴化物的化学式为PBr3,中心原子的价层电子对数是4,有1对孤对电子,所以空间构型为三角锥型 (2)根据题目中提供的合成BG的条件,则合成BG的化学反应方程式为BBr3+PBr3+3H2 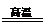  BP+6HBr BP+6HBr(3)B原子位于P的正四面体的中心,所以B与P的最近距离是正四面体的中心到顶点的距离,设立方体的棱长为b,则 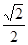 b× b×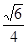 =a,b= =a,b=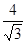 a,该晶胞中实际拥有4个BP,所以该晶胞的密度为4×42/NA/( a,该晶胞中实际拥有4个BP,所以该晶胞的密度为4×42/NA/(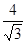 a×10-10)3= a×10-10)3=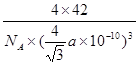 |
相似问题
下列关于化合价的判断正确的是 [ ]A.Na2O中O元素为-1价
下列关于化合价的判断正确的是 [ ]A Na2O中O元素为-1价B Na2O2中O元素为-2价 C SO2中O元素为-1价D SO3中O元素为-2价
下列各组物质各自形成的晶体 均属于分子晶体的化合物的是( )。A.NH3 HD C10H8
下列各组物质各自形成的晶体,均属于分子晶体的化合物的是()。A.NH3、HD、C10H8B.PCl3、CO2、H2SO4C.SO2、SiO2、P2O5D.CCl4、Na2S、H2O2
现有1——20号元素A B C D所对应的物质的性质或微粒结构如下表:元素物质性质或微粒结构AM层上
现有1——20号元素A、B、C、D所对应的物质的性质或微粒结构如下表:元素物质性质或微粒结构AM层上有2对成对电子BB的离子与D的离子具有相同电子层结构,且
MnO2是碱锰电池材料中最普通的正极材料之一 在活性材料MnO2中加入CoTiO3纳米粉体 可以提高
MnO2是碱锰电池材料中最普通的正极材料之一,在活性材料MnO2中加入CoTiO3纳米粉体,可以提高其利用率,优化碱锰电池的性能。(1)写出基态Mn原子的核外电子排
X元素最高氧化物对应的水化物为H3XO4 则它对应的气态氢化物为[ ]A.HXB.H2X C
X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为[ ]A.HXB.H2X C.XH4 D.XH3












