现有1——20号元素A B C D所对应的物质的性质或微粒结构如下表:元素物质性质或微粒结构AM层上
现有1——20号元素A、B、C、D所对应的物质的性质或微粒结构如下表:
(1)元素A的原子最外层共有______种不同运动状态的电子,有___种能量不同的电子。B的 离子与D的离子相互组合形成的干燥剂的化学式是_________。 (2)元素C与氢元素形成带一个单位正电荷的离子,写出该微粒的电子式(用元素符号表示) _________________ (3)元素A与元素D相比,非金属性较强的是_____(用元素符号表示),下列表述中能证明 这一事实的是_______ A.常温下A的单质和D的单质状态不同 B.A的氢化物比D的氢化物稳定 C.一定条件下D能从A的氢化物水溶液中置换出A单质 D.HD的酸性比HA酸性强 (4)C的氢化物固态时属于______晶体,该氢化物与A的最高价氧化物水化物反应的化学方程式是__________________________________________________。 |
参考解答
| (本题共8分,每空1分) (1)6,2,CaCl2 (2) 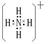 (3)Cl,C (4)分子,2NH3+H2SO4→(NH4)2SO4 |
试题分析:M层上有2对成对电子可推出A原子3P轨道分布了4个电子,为S;根据C的氢化物水溶液呈碱性可知C为N;1—20号元素元素最高正价是+7价只有Cl,所以D为Cl元素;B的离子与D的离子具有相同电子层结构,且可以相互组合形成干燥剂,可推出D为Ca元素。 (1)S原子最外层为6个电子,既有6种电子运动状态,分布在3S、3P轨道上,有2种能量不同的电子,Cl ̄与Ca2+形成的干燥剂为CaCl2。 (2)N元素与氢元素形成带一个单位正电荷的离子为NH4+。 (3)根据元素周期律和元素周期表,Cl的非金属性大于S;一定条件下Cl2能从H2S水溶液中置换出S单质,说明Cl原子的得电子能力大于S原子,Cl元素的非金属性大于S元素。 (4)C的氢化物为NH3,固态时属于分子晶体,A的最高价氧化物水化物为H2SO4,二者反应生成(NH4)2SO4。 |
相似问题
MnO2是碱锰电池材料中最普通的正极材料之一 在活性材料MnO2中加入CoTiO3纳米粉体 可以提高
MnO2是碱锰电池材料中最普通的正极材料之一,在活性材料MnO2中加入CoTiO3纳米粉体,可以提高其利用率,优化碱锰电池的性能。(1)写出基态Mn原子的核外电子排
X元素最高氧化物对应的水化物为H3XO4 则它对应的气态氢化物为[ ]A.HXB.H2X C
X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为[ ]A.HXB.H2X C.XH4 D.XH3
材料是人类赖以生存的重要物质基础。铜 镍等金属材料在现代社会中有着重要应用。请回答下列问题:(1)铜
材料是人类赖以生存的重要物质基础。铜、镍等金属材料在现代社会中有着重要应用。请回答下列问题:(1)铜在元素周期表中的位置为,镍的基态电子排布式为
我国已研制出一种稀土制冷材料 其主要成分是LaCaMnO。(1)锰原子的基态价层电子排布式为____
我国已研制出一种稀土制冷材料,其主要成分是LaCaMnO。(1)锰原子的基态价层电子排布式为________。(2)S与O为同主族元素,其中电负性较大的是________
已知某元素的氧化物的相对分子质量为40 其相同价态氯化物的相对分子质量为95 则该元素的化合价为(
已知某元素的氧化物的相对分子质量为40,其相同价态氯化物的相对分子质量为95,则该元素的化合价为( )A.-2B.+1C.+2D.+3












