(14分)下图是元素周期表的一部分① ② ③④
(14分)下图是元素周期表的一部分
(2)如果在温度接近373K时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是 。 (3)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质。写出元素②的氢氧化物与NaOH溶液反应的离子方程式 。 (4)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
②T元素最可能是 (填“s”、“p”、“d”、“ds”等)区元素,位于 族;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为 。 |
参考解答
(1) 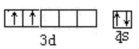 ;14 (2)分子间存在氢键,H2O分子发生缔合 ;14 (2)分子间存在氢键,H2O分子发生缔合(3)2OH— + Be(OH)2=BeO22—+ 2H2O (4)①R 和U ② p(1分) IIIA(1分)120° |
试题分析:(1)根据元素在周期表中的位置可知,元素⑨是钛元素,原子序数是22,因此根据核外电子排布规律其知的价电子轨道表示式为  。元素⑩是铁,其次外层电子数为14个。 。元素⑩是铁,其次外层电子数为14个。(2)元素⑤是水,水分子间存在氢键,H2O分子发生缔合,因此测定结果比理论值高。 (3)②、⑦分别是Be和Al,氢氧化铝是两性氢氧化物,则元素②的氢氧化物与NaOH溶液反应的离子方程式为2OH— + Be(OH)2=BeO22—+ 2H2O。 (4)由元素的电离能可以看出,Q的电离能很大,可能为零族元素,R和U的第一电离能较小,第二电离能剧增,故表现+1价,最外层电子数为1,二者位于同一族,S的第一、第二电离能较小,第三电离能剧增,故表现+2价,最外层电子数为2,T的第一、第二、第三电离能较小,第四电离能剧增,表现+3价,最外层电子数为3,则 ①由上述分析可知,R和U的第一电离能较小,第二电离能剧增,故表现+1价,最外层电子数为1,二者位于同一族。 ②由上述分析可知,T的第一、第二、第三电离能较小,第四电离能剧增,表现+3价,最外层电子数为3,可能为P区元素,位于第ⅢA族;若T为第二周期元素,则T是B元素。Z是第三周期元素中原子半径最小的主族元素,因此Z是氯元素,则T、Z形成的化合物是BCl3,B原子的价层电子对数是3个,且不存在孤对电子,所以是平面三角形结构,分子键角为120°。 |
相似问题
元素A和B的原子序数都小于18。已知A元素原子的最外层电子数为a 次外层电子数为b;B元素原子的M层
元素A和B的原子序数都小于18。已知A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为(a-b),L层电子数为(a+b),则A、B两元素所形
(14分)现有5种短周期元素A B C D E 原子序数依次增大。A的同位素中有一种核素无中子 B最
(14分)现有5种短周期元素A、B、C、D、E,原子序数依次增大。A的同位素中有一种核素无中子,B最外层上电子数是次外层电子数的两倍,C元素最简单的氢化物
(12分)A B C D E五种短周期元素 其原子序数依次增大 而原子半径按A C B E D顺序依
(12分)A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D顺序依次增大。A、D同主族;B、D、E三种元素原子的最外层电子数之
以下有关原予结构及元素周期律的叙述正确的是A.同主族元素从上到下 单质的熔点逐渐降低B.同周期元素(
以下有关原予结构及元素周期律的叙述正确的是A.同主族元素从上到下,单质的熔点逐渐降低B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小C.第
X元素的阳离子与Y的阴离子具有相同的核外电子排布 则下列比较中正确的是( ) A.原子序数:
X元素的阳离子与Y的阴离子具有相同的核外电子排布,则下列比较中正确的是( )A.原子序数: X<YB.原子半径:X<YC.离子半径:X>YD.原子最外层电子数:X<Y












