C N O是中学化学常见的三种元素 请回答下列问题:(1)写出基态O2-的核外电子排布式______
| C、N、O是中学化学常见的三种元素,请回答下列问题: (1)写出基态O2-的核外电子排布式______________________________。 (2)C、N、O三种元素的第一电离能由大到小的顺序为_____________________________。 (3)光气( 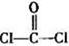 )分子中含有______个 )分子中含有______个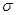 键,____个 键,____个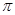 键,其中C原子的杂化方式为_______。 键,其中C原子的杂化方式为_______。(4)水的熔点比H2S的熔点高,其原因是________________。 (5)超硬材料氮化销的晶胞如图 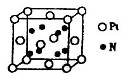 所示,则氮化铂的化学式为_______。 所示,则氮化铂的化学式为_______。 |
参考解答
| (除注明外,每空1分,共8分)(1)1s22s22p6 (2)3;1;sp2 (4)H2O分子间形成氢键 (5)PtN2 |
试题分析:(1)O2-核外有10个电子,根据构造原理可知,其核外电子排布式为1s22s22p6。 (2)同周期第一电离能自左而右具有增大趋势,所以第一电离能O>C。由于氮元素原子2p能级有3个电子,处于半满稳定状态,能量较低,第一电离能大于相邻元素,所以B、C、D三种元素的第一电离能数值由大到小的顺序为N<O<C。 (3)单键都是σ 键,双键是由一个σ 键和1个π键构成的。所以根据光气的结构式可知,光气分子中含有3σ键,一个π键,碳原子含有3个σ 键且不含孤电子对,所以其杂化方式为sp2。 (4)O、S属于同一主族元素,硫化氢的相对分子质量大于水,但水中含有氢键,导致水的熔点比H2S的熔点高。 (5)根据晶胞结构并依据均摊法可知,N原子个数=8个,Pt原子个数=8× 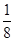 +6× +6×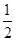 =4个,所以其化学式为PtN2。 =4个,所以其化学式为PtN2。 |
相似问题
[化学—选修3:物质结构与性质](15分)有A B C D E F G H原子序数递增的前四周期八种
[化学—选修3:物质结构与性质](15分)有A、B、C、D、E、F、G、H原子序数递增的前四周期八种元素。请根据下列信息,回答问题:①A、B、C、D、E、F为短周
下列各项比较中前者高于(或大于或强于)后者的是A.CCl4和SiCl4的熔点B.邻羟基苯甲醛()和对
下列各项比较中前者高于(或大于或强于)后者的是A.CCl4和SiCl4的熔点B.邻羟基苯甲醛()和对羟基苯甲醛()的沸点C.SO2和CO2在水中的溶解度D.H2SO3和H2SO4的酸性
原子序数依次增大的短周期元素a b c d和e中 a的最外层电子数为其周期数的二倍;b和d的A2B型
原子序数依次增大的短周期元素a、b、c、d和e中,a的最外层电子数为其周期数的二倍;b和d的A2B型氢化物均为V型分子,c的+1价离子比e的﹣1价离子少8个电子
【化学选修-物质结构与性质】(15分)已知前四周期六种元素A B C D E F的原子序数之和为10
【化学选修-物质结构与性质】(15分)已知前四周期六种元素A、B、C、D、E、F的原子序数之和为107,且它们的核电荷数依次增大。B原子的p轨道半充满,其氢化
碳 氮 氧是构成生命物质的三种主要元素。(1)碳 氮 氧三种元素中 原子核外电子未成对电子数最多的是
碳、氮、氧是构成生命物质的三种主要元素。(1)碳、氮、氧三种元素中,原子核外电子未成对电子数最多的是________(用元素符号表示)。(2)已知CN-与N












