A B C D E是短周期元素 周期表中A与B B与C相邻 且C与E同主族;A与E的最外层电子数之比
| A、B、C、D、E是短周期元素,周期表中A与B、B与C相邻,且C与E同主族;A与E的最外层电子数之比2:3,B的最外层电子数比C的最外层电子数少1个;常见化合物D2C2与水反应生成C的单质,且溶液使酚酞试液变红. (1)E的元素名称是______.该元素在周期表中的位置为______ (2)A、B、C的氢化物稳定性由弱到强的顺序为(用分子式表示)______;B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z中所含化学键的类型为______ (3)写出D2C2的电子式______.用电子式表示只含D、E两种元素的化合物的形成过程______ (4)写出D2C2与H2O反应的离子方程式______. |
参考解答
| 根据常见化合物D2C2与水反应生成C的单质,且溶液使酚酞试液变红,可知C为O元素,D为Na元素,B的最外层电子数比C的最外层电子数少1个,则B的最外层电子数为5,且相邻,应为N元素,C与E同主族,E应为S元素,A与B相邻,A与E的最外层电子数之比2:3,则A的最外层电子数为4,应为C元素. (1)E为S元素,原子序数为16,核外有3个电子层,最外层电子数为6,位于周期表第三周期VIA族, 故答案为:硫;第三周期VIA族; (2)A、B、C分别为C、N、O元素,同一周期元素从左到右元素的非金属性逐渐增强,对应的氢化物的稳定性逐渐增大,A、B、C的氢化物稳定性由弱到强的顺序为CH4<NH3<H2O,B的氢化物和B的最高价氧化物的水化物反应生成Z,则Z为NH4NO3,为离子化合物,含有离子键、极性键,故答案为:CH4<NH3<H2O;离子键、极性键; (3)Na2O2为离子化合物,电子式为 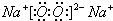 ,D和E形成的化合物为Na2S,为离子化合物,用电子式表示的形成过程为 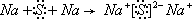 ,故答案为: 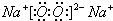 ; 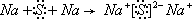 ; (4)Na2O2与水反应生成NaOH和氧气,反应的离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑, 故答案为:2Na2O2+2H2O=4Na++4OH-+O2↑. |
相似问题
有X Y Z W M五种短周期元素 它们满足如下关系:①原子序数依次增大;②ZX4++WX-=ZX3
有X、Y、Z、W、M五种短周期元素,它们满足如下关系:①原子序数依次增大;②ZX4++WX-=ZX3+X2W,且反应物和产物中各微粒的电子总数与M+相等,均为10个;③
已知X Y Z W四种短周期元素的原子序数依次增大 其中X与Y Z W所形成的常见化合物在常温下均呈
已知X、Y、Z、W四种短周期元素的原子序数依次增大,其中X与Y、Z、W所形成的常见化合物在常温下均呈气态,在周期表中W与Z左右相邻,Y的最高价氧化物对应的
A B C三种元素的原子具有相同的电子层数 且B的核外电子数比A多2个 C的质子数比B多4个 1mo
A、B、C三种元素的原子具有相同的电子层数,且B的核外电子数比A多2个,C的质子数比B多4个,1molA的单质与酸反应,能置换出1gH2,这时,A转化为具有氖原子
有A B C D四种短周期元素 它们的原子序数由A到D依次增大 已知A和B原子有相同的电子层数 且A
有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的一种单质硬度很大,C燃烧时使火焰呈现黄色,C的单质在
A B C D E F六种主族元素分布在三个短周期 它们的原子序数依次增大.其中B与C位于同二周期
A、B、C、D、E、F六种主族元素分布在三个短周期,它们的原子序数依次增大.其中B与C位于同二周期,A与D、C与F分别位于同一主族,A与D两元索核外电子数之












