在有机化学工业中常用的一种钠盐是NaBH4 即硼氢化钠。它具有很强的还原性 也是一种高贮氢密度材料
| 在有机化学工业中常用的一种钠盐是NaBH4,即硼氢化钠。它具有很强的还原性,也是一种高贮氢密度材料,是最有可能作为氢燃料电池的即时供应氢源。但它不能与水和酸共存。 ⑴将其投入水中可生成偏硼酸钠(NaBO2)和氢气,写出该反应的化学方程式 ,反应中的还原剂是 ,每摩NaBH4反应时电子转移数为 mol。 ⑵若将NaBH4投入酸溶液中其反应速率与其放入水中相比,应快还是慢 ,理由是 。 ⑶NaBH4还用于将含Au3+的碱性废液中回收黄金,其离子方程式为: 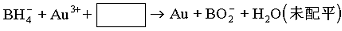 请写出配平的离子方程式 。 |
参考解答
| ⑴NaBH4+2H2O=NaBO2+4H2↑ NaBH4 4 ⑵快,因BH4-与H2O中的H+反应为反应实质,酸中H+浓度比水中大,生成H2的速率要比在水中的快。 ⑶3BH4-+8Au3++24OH-=8Au+3BO2-+18H2O (1,1,1,1,1,1) |
| 略 |
相似问题
向盛有KI溶液的试管中加入少许CCl4后滴加氯水 CCl4层变成紫色。如果继续向试管中滴加氯水 振荡
向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:(1)写
在8NH3+3Cl2=N2+6NH4Cl反应中 若有21.3g Cl2参加反应 则被氧化的NH3的质
在8NH3+3Cl2=N2+6NH4Cl反应中,若有21.3g Cl2参加反应,则被氧化的NH3的质量为()A.13.6gB.10.2gC.6.8gD.3.4g
某反应体系的物质有:H2SO4 KMnO4 MnSO4 CO2 K2C2O4 K2SO4 H2O.(
某反应体系的物质有:H2SO4、KMnO4、MnSO4、CO2、K2C2O4、K2SO4、H2O.(已知CO2为生成物)(1)将上述物质填入以下空格内,组成一个配平的化学反应方程
标准状况下 a L Cl2通入到1 Lb mol/L的FeI2溶液中 充分反应后 所得溶液中Fe2+
标准状况下,a L Cl2通入到1 Lb mol L的FeI2溶液中,充分反应后,所得溶液中Fe2+的物质的量浓度与a、b的关系如下表,请完成其余空格。a、b的关系Fe2
(1)写出实验室制NH3的反应方程式为______;(2)硝酸具有强氧化性 它能和许多物质发生反应.
(1)写出实验室制NH3的反应方程式为______;(2)硝酸具有强氧化性,它能和许多物质发生反应.写出浓硝酸与非金属单质碳的反应方程式.______.配平下列












