在AlCl3和FeCl3的混合液中 先加入过量的KI溶液 再加入足量的Na2S溶液 所得到的沉淀物是
在AlCl3和FeCl3的混合液中,先加入过量的KI溶液,再加入足量的Na2S溶液,所得到的沉淀物是( )
|
参考解答
| 在FeCl3和AlCl3溶液中加过量KI,先是FeCl3与KI两盐发生氧化还原反应:2Fe3++2I-=2Fe2++I2,反应完后溶液中含大量Fe2+、Al3+、I2, 再加入Na2S后,由于S2-+H2O 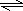 HS-+OH-.在Na2S溶液中,有大量S2-、OH-,依题意知,Fe2+结合S2-能力强,两盐发生复分解反应,形成FeS沉淀, Fe2++S2-=FeS↓;Al3+结合OH-能力强,形成Al(OH)3沉淀,Al3++3OH-=Al(OH)3↓,或理解为Al3+与S2-发生双水解反应:3Na2S+AlCl3+6H2O=2Al(OH)3↓+3H2S↑+6NaCl; 但由于I2的存在发生:I2+S2-=S↓+2I-或I2+H2S=S↓+2HI,所以最终得到的沉淀是FeS、Al(OH)3和S的混合物. 故选D. |
相似问题
钡与钠相似 也能形成含O22-的过氧化物 下列叙述中正确的是( )A.过氧化钡的化学式为Ba2O2
钡与钠相似,也能形成含O22-的过氧化物,下列叙述中正确的是( )A.过氧化钡的化学式为Ba2O2B.O22-的电子式为:C.反应Na2O2+2HCl═2NaCl+H2O2为氧
(1)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜 制造印刷电路板.请写出FeCl3溶液
(1)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板.请写出FeCl3溶液与铜反应的化学方程式:______.检验反应后的溶液中存在Fe3+
某100mL的CuCl2溶液中 已知溶液中的Cl-的浓度为0.2mol?L-1.现将一定量的铁粉投入
某100mL的CuCl2溶液中,已知溶液中的Cl-的浓度为0 2mol?L-1.现将一定量的铁粉投入到该溶液中,若反应后溶液体积不变,回答下列问题:(1)原溶液中Cu2+
向盛有KI溶液的试管中加入少许CCl4后滴加氯水 CCl4层变成紫色.如果继续向试管中滴加氯水 振荡
向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色.如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色.完成下列填空:(1)
下列反应中 既是化合反应 又是氧化还原反应的是( )①过氧化钠与水反应 ②钠在氧气中燃烧 ③
下列反应中,既是化合反应,又是氧化还原反应的是( )①过氧化钠与水反应②钠在氧气中燃烧③氧化钙与水反应④CO燃烧⑤铁粉与FeCl3溶液反应.A.①②












