已知乙二酸(HOOC-COOH 可简写为H2C2O4)俗称草酸 易溶于水 属于二元中强酸(为弱电解质
| 已知乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华.某校研究性学习小组为探究草酸的部分化学性质,进行了如下实验: (1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为______. (2)向盛有少量乙二酸饱和溶液的试管中滴入用硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明乙二酸具有______(填“氧化性”、“还原性”或“酸性”),请配平该反应的离子方程式: ______ MnO4-+______ H2C2O4+______ H+=______ Mn2++______ CO2↑+______ H2O (3)将一定量的乙二酸放于试管中,按如图所示装置进行实验(夹持装置未标出): 实验发现,装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红, 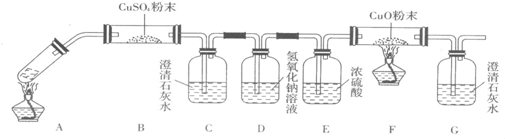 据此,乙二酸分解的产物为______.上述装置中,D的作用是______. 装置F中发生反应的化学方程式为:______. (4)该小组同学将2.52g草酸晶体(H2C2O4?2H2O)加入到100mL 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是______. |
参考解答
| (1)乙二酸中含有羧基,具有酸性,酸性比碳酸强,与碳酸氢钠反应生成二氧化碳和乙酸钠,该反应的离子方程式为:HCO3-+H2C2O4=HC2O4-+CO2↑+H2O; (2)酸性KMnO4溶液具有强氧化性,向盛有少量乙二酸饱和溶液的试管中滴入用硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明乙二酸被酸性高锰酸钾氧化,具有还原性; 根据氧化还原反应方程式的配平原则:得失电子守恒、质量守恒和电荷守恒配平该反应的离子方程式:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O; (3)加热乙二酸,反应物通入B,使CuSO4粉末变蓝,说明有水生成,装置C中澄清石灰水变浑浊,说明有二氧化碳生成;装置D中二氧化碳和氢氧化钠反应除去混合气体中的二氧化碳,F中CuO粉末变红、G中澄清石灰水变浑浊说明有一氧化碳生成,所以乙二酸的分解产物为CO、CO2、H2O;装置F中发生的反应为一氧化碳还原氧化铜,化学方程式为:CuO+CO
(4)2.52g草酸晶体的物质的量=
100mL 0.2mol/L的NaOH溶液中氢氧化钠的物质的量=100mL×10-3L/mL×0.2mol/L=0.02mol; 所以反应生成NaHC2O4,所得溶液为NaHC2O4溶液,由于HC2O4-的电离程度比水解程度大,导致溶液中c(H+)>c(OH-),所以溶液呈酸性. 故答案为:(1)HCO3-+H2C2O4=HC2O4-+CO2↑+H2O; (2)还原性,2、5、6、2、10、8; (3)CO、CO2、H2O,除去混合气体中的CO2,CuO+CO
(4)反应所得溶液为NaHC2O4溶液,由于HC2O4-的电离程度比水解程度大,导致溶液中c(H+)>c(OH-),所以溶液呈酸性. |
相似问题
KClO3和浓HCl在一定温度下反应会生成黄绿色的易爆物二氧化氯.其反应可表述为:______KCl
KClO3和浓HCl在一定温度下反应会生成黄绿色的易爆物二氧化氯.其反应可表述为:______KClO3+______HCl(浓)→______KCl+______ClO2+______Cl2+______H2O
金属钙线是炼制优质钢材的脱氧脱磷剂 某钙线的主要成分为金属M和Ca 并含有3.5%(质量分数)CaO
金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和Ca,并含有3 5%(质量分数)CaO(1)Ca元素在周期表中位置是______,其原子结构示意图__
古老但仍然是最有用的制备联氨(N2H4)溶液的方法如下:NaClO+NH3?H2O→N2H4+NaC
古老但仍然是最有用的制备联氨(N2H4)溶液的方法如下:NaClO+NH3?H2O→N2H4+NaCl+H2O(1)请配平上述化学方程式.并用单线桥法标出电子转移的方向和数目
(1)①配平下列离子方程式:_____I-x+_____Cl2+_____H2O→____Cl-+_
(1)①配平下列离子方程式:_____I-x+_____Cl2+_____H2O→____Cl-+____IO3-+_______②在反应中,若消耗I-x与Cl2物质的量之比为1∶8,则x=___________。
用干燥的高锰酸钾可以制得极纯而干燥的氧气:KMnO4MnO2+K2O+O2(240 ℃)。下列说法不
用干燥的高锰酸钾可以制得极纯而干燥的氧气:KMnO4MnO2+K2O+O2(240 ℃)。下列说法不正确的是( )A.每生成16 g氧气转移4 mol电子B.相同质量的KMnO4分












