2010年上海世博会场馆 大量的照明材料或屏幕都使用了发光二极管(LED)。目前市售LED品片 材质
2010年上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED)。目前市售LED品片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、lnGaN(氮化铟镓)为主。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如图。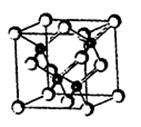 试回答: ⑴镓的基态原子的电子排布式是 。 ⑵砷化镓晶胞中所包含的砷原子(白色球)个数为 ,与同一个镓原子相连的砷原子构成的空间构型为 。 ⑶N、P、As处于同一主族,其氢化物沸点由高到低的顺序是 。 (用氢化物分子式表示) ⑷砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为 。 ⑸比较二者的第一电离能:As______Ga(填“<”、“>”或“=”)。 ⑹下列说法正确的是 (填字母)。 A.砷化镓晶胞结构与NaCl相同 B.GaP与GaAs互为等电子体 C.电负性:As>Ga D.砷化镓晶体中含有配位键 |
参考解答
| ⑴l s22s22p63s23p63d104s24p1(或[Ar3d104s24p1) ⑵4 正四面体 ⑶NH3>AsH3>PH3 ⑷sp2 ⑸> ⑹BCD |
试题分析:⑴31号元素镓的基态原子的电子排布式是l s22s22p63s23p63d104s24p1(或[Ar3d104s24p1)⑵砷化镓晶胞中所包含的砷原子(白色球)个数为8×1/8+6×1/2='4;' 与同一个镓原子相连的砷原子构成的空间构型为正四面体型⑶N、P、As处于同一主族,其氢化物都是分子晶体。结构相似,对于结构相似的物质来说,相对分子质量越大。分子间的作用力就越大,克服分子间作用力使物质融化或汽化需要的能量就越高。即熔沸点越高。但由于氨气的分子之间还存在氢键,增加了分子之间的相互作用,使的它的熔沸点比AsH3还高。因此N、P、As的氢化物沸点由高到低的顺序是NH3>AsH3>PH3。(4)(CH3)3Ga中镓原子的杂化方式为sp2⑸As是33号元素,它的核外电子排布是l s22s22p63s23p63d104s24p3,p轨道处于半充满的稳定状态。所以As 、Ga 第一电离能:As>Ga 。⑹A.砷化镓和NaCl晶体结构不同。错误。B.GaP与GaAs互为等电子体。正确。C.同一周期的元素随着原子序数的增大,元素的非金属性逐渐增强,其电负性也逐渐增大。所以电负性:As>Ga。正确。D.砷是VA族元素,最外层5个电子,镓是IIIA族,最外层有三个电子,砷和镓先形成3个σ键。此时砷有一对孤对电子,镓有一个空轨道,可以形成一个配位键。正确。选项为:BCD。 |
相似问题
A D E X Y五种短周期元素 它们的原子序数依次增大 A元素的原子是半径最小的原子 D元素的最高
A、D、E、X、Y五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子,D元素的最高价氧化物对应的水化物与其氢化物反应生成一种盐;X与A
A B是短周期VIIA族的两种元素 A的非金属性比B强。下列关于A B的说法正确的是A.A元素的单质
A、B是短周期VIIA族的两种元素,A的非金属性比B强。下列关于A、B的说法正确的是A.A元素的单质可以把B元素的单质从NaB溶液中置换出来B.NaA、NaB的晶体都
A B C D E F为前四周期元素且原子序数依次增大 其中A含有3个能级 且每个能级所含的电子数相
A、B、C、D、E、F为前四周期元素且原子序数依次增大,其中A含有3个能级,且每个能级所含的电子数相同;C的最外层有6个运动状态不同的电子;D是短周期元素中电
I.下列说法中正确的是 。A.第一电离能由大到小的顺序为O>N>CB.由于C和O互为
I.下列说法中正确的是。A.第一电离能由大到小的顺序为O>N>CB.由于C和O互为等电子体,所以可以推断O的电子式为C.根据岩浆晶出规则,Ca0比Mg0更容易在
漂白精的有效成分是NaClO 其所含氯元素的化合价为[ ]A.2 B.+1 C.-1 D.
漂白精的有效成分是NaClO,其所含氯元素的化合价为[ ]A.2 B.+1 C.-1 D.+2












