A B C D E为原子序数依次增大的五种短周期元素。A和D最外层电子数相同;C E最低负价相同。B
| A、B、C、D、E为原子序数依次增大的五种短周期元素。A和D最外层电子数相同;C、E最低负价相同。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的化合物甲和乙(相对分子质量甲<乙),D2C中阳离子与阴离子的电子层结构相同。请回答下列问题: (1)B的氢化物与E的氢化物比较,沸点较高的是 (填化学式)。 (2)已知乙能与由A、C、D组成的化合物的溶液反应,请写出反应的离子方程式 。 (3)A、B两种元素可形成一种离子化合物,该离子化合物的电子式为 。 (4)向A、B、C三种元素组成的某盐溶液中滴加AgNO3溶液生成白色沉淀,该反应的化学方程式为____________。已知该盐溶液呈酸性,0.1mol·L-1该盐溶液中离子浓度由大到小的顺序是_________________________。 (5)化合物X、Y由A、C、D、E四种元素中的三种组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1∶1∶1,若X能抑制水的电离,Y能促进水的电离,则X与Y反应的离子方程式是 。 |
参考解答
| (1)NH3 (2)H2O2+OH-=HO2-+H2O HO2-+OH-=H2O+O22- (或H2O2+2OH-=O22-+2H2O) (3) 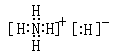 (4)NH4NO2+AgNO3=AgNO2↓+NH4NO3 c(NO2-)>c(NH4+)>c(H+)>c(OH-) (5)HS-+OH-=S2-+H2O |
| 根据元素的结构及有关性质可知,A、B、C、D、E五种元素分别是H、N、O、Na、S。 (1)NH3的沸点比H2S的要高。 (2)过氧化氢可以看作是二元弱酸,所以和氢氧化钠反应的方程式为H2O2+2OH-=O22-+2H2O。 (3)H和N要形成离子化合物,则只能是氢化铵,其电子式为 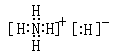 (4)硝酸银易溶于水,所以白色沉淀应该是亚硝酸银,方程式为NH4NO2+AgNO3=AgNO2↓+NH4NO3;溶液显酸性,说明NH4+的水解程度大于NO2-的水解程度,所以离子浓度大小顺序是c(NO2-)>c(NH4+)>c(H+)>c(OH-)。 (5)根据XY的性质及组成结构特点可知,X是NaOH,Y是NaHS,二者反应的方程式为HS-+OH-=S2-+H2O。 |
相似问题
已知A B C D E F为元素周期表中原子序数依次增大的前20号元素 A B与C;D E与F分别位
已知A、B、C、D、E、F为元素周期表中原子序数依次增大的前20号元素,A、B与C;D、E与F分别位于同一周期。A原子L层上有3个未成对电子,B的简单负二价离子
已知1~18号元素的离子aW3+ bX+ cY2- dZ- 都具有相同的电子层结构 下列关系正确的是
已知1~18号元素的离子aW3+、bX+、cY2-、dZ- 都具有相同的电子层结构,下列关系正确的是A.质子数:c>bB.离子的还原性:Y2->Z-C.氢化物的稳定性:H2Y
下列说法中错误的是 A.SO2 SO3都是极性分子B.在NH4+和[Cu(NH3)4]2+中都存在配
下列说法中错误的是 A.SO2、SO3都是极性分子B.在NH4+和[Cu(NH3)4]2+中都存在配位键C.元素电负性越大的原子,吸引电子的能力越强 D.PCl3和NF3分子
(双选)某元素X的原子序数为52 下列叙述正确的是( )。A.X的主要化合价是-2 +4 +6B.
(双选)某元素X的原子序数为52,下列叙述正确的是( )。A.X的主要化合价是-2、+4、+6B.X可以形成稳定的气态氢化物C.X的最高价氧化物对应水化物的酸性
(16分)已知A B C D E F G和H都是元素周期表中前36号的元素 它们的原子序数依次增大。
(16分)已知A、B、C、D、E、F、G和H都是元素周期表中前36号的元素,它们的原子序数依次增大。A是周期表中原子半径最小的元素,B原子最外层电子数是内层












