(10分)(2011·锦州高一检测)目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下:请
(10分)(2011·锦州高一检测)目前世界上60%的镁是从海水提取的。海水提镁的主要流程如下: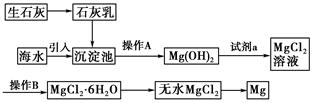 请回答下列问题: (1)从离子反应的角度思考,在海水中加入石灰乳的作用是________,写出在沉淀池发生反应的离子方程式 ________________________________________________________. (2)石灰乳是生石灰与水形成的化合物,从充分利用海洋化学资源,提高经济效益的角度考虑,生产生石灰的主要原料来源于海洋中的________________________。 (3)操作A是________,操作B是________。 (4)加入的足量试剂a是________(填化学式)。 (5)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为______________________________________________________________________。 从考虑成本和废物循环利用的角度,副产物氯气可以用于 __________________________________________________________________。 |
参考解答
| (1)沉淀Mg2+[或使Mg2+形成Mg(OH)2沉淀 Mg2++2OH-===Mg(OH)2↓ (2)贝壳(或牡蛎壳等) (3)过滤 加热浓缩(或蒸发结晶) (4)HCl (5)MgCl2(熔融)  Mg+Cl2↑ 制盐酸,循环使用 Mg+Cl2↑ 制盐酸,循环使用 |
| (1)石灰乳中含有OH-,能结合镁离子生成氢氧化镁沉淀,方程式为Mg2++2OH-===Mg(OH)2↓。 (2)由于贝壳的主要成分就是碳酸钙,因此可以利用海洋中的贝壳等。 (3)要得到沉淀,应该通过过滤;氯化镁易溶于水,因此要得到氯化镁晶体,应该是加热浓缩(或蒸发结晶)。 (4)氢氧化镁要转化为氯化镁,需要加入盐酸。 (5)镁是活泼的金属,通过电解法冶炼,方程式为MgCl2(熔融)  Mg+Cl2↑;氯气可以制取盐酸,循环使用。 Mg+Cl2↑;氯气可以制取盐酸,循环使用。 |
相似问题
能用分液漏斗分离的混合物是( )A.液溴和四氯化碳B.苯和蒸馏水C.乙醛和乙醇D.溴苯和苯
能用分液漏斗分离的混合物是()A.液溴和四氯化碳B.苯和蒸馏水C.乙醛和乙醇D.溴苯和苯
气体X可能由NH3 Cl2 HBr CO2中的一种或几种组成 已知X通入AgNO3溶液时产生浅黄色沉
气体X可能由NH3、Cl2、HBr、CO2中的一种或几种组成,已知X通入AgNO3溶液时产生浅黄色沉淀,该沉淀不溶于稀HNO3,若将X通入澄清石灰水中,无沉淀产生,则
粗食盐中除含有钙离子 镁离子 硫酸根离子等可溶性杂质外 还含有泥砂等不溶性杂质。我们食用的精盐是用粗
粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥砂等不溶性杂质。我们食用的精盐是用粗食盐提纯而得到的。通过教材中“粗盐的提纯”
(12分)已知某工业废水中含有大量FeSO4 较多的Cu2+ 少量的Na+ 以及部分污泥 通过下列流
(12分)已知某工业废水中含有大量FeSO4,较多的Cu2+,少量的Na+ 以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu。(1)步骤1、步
提纯含有少量Ba(NO3)2杂质的KNO3溶液 可以使用的方法为( )A.加入过量的K2SO4溶液
提纯含有少量Ba(NO3)2杂质的KNO3溶液,可以使用的方法为( )A.加入过量的K2SO4溶液,过滤,向滤液中滴加适量的稀硝酸B.加入过量的Na2CO3溶液,过滤,












