核事故时往往泄漏出污染物(具有放射性的碘原子)。为避免核辐射 需一次性口服100毫克不具放射性的碘原
| 核事故时往往泄漏出污染物(具有放射性的碘原子)。为避免核辐射,需一次性口服100毫克不具放射性的碘原子,使人体甲状腺中碘达到饱和而不再吸收外界的碘,从而起到保护作用。假设所处的环境已受污染,通过服用加碘食盐的方法能否有效起到避免核辐射的目的呢? 【查阅资料】成人每天食用食盐的质量通常为6g;某种加碘食盐的标签如图所示。 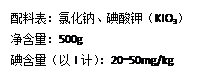 ⑴碘酸钾(KIO3)的相对分子质量为___________; ⑴碘酸钾(KIO3)的相对分子质量为___________;⑵碘酸钾中K︰I︰O的元素质量比为___________; ⑶碘酸钾中碘元素的质量分数为___________; ⑷每袋加碘盐至少含碘酸钾多少毫克? (要求:写出必要的计算步骤,计算结果保留一位小数) 【问题分析】若要使人体甲状腺中的碘达到饱和,至少需要一次性食用该品牌碘盐____kg。 【结论】日常服用加碘食盐_①_(填“能”或“不能”)起到避免核辐射目的,原因是___②__。 |
参考解答
| 【查阅资料】⑴214 ⑵K︰I︰O = 39︰127︰48 ⑶59.3% 解:KIO3的质量为:20mg÷59.3%≈33.7mg 【问题分析】2 Kg 【结论】①不能②因为每天食用食盐约为6g,远小于2㎏ (其他合理答案也可) |
| 分析:(1)根据碘酸钾的化学式KIO3,利用各元素的相对原子质量进行计算; (2)根据碘酸钾的化学式,可计算组成元素的质量比; (3)根据碘酸钾的化学式,可计算组成元素的质量分数; (4)根据净含量及碘含量来计算每袋加碘盐至少含碘酸钾的质量,并根据成人每天食用食盐的质量通常为6g来分析能否有效起到避免核辐射. 解答:解:(1)碘酸钾KIO3的相对分子质量=39+127+16×3=214; (2)KIO3中钾元素、碘(I)元素、氧元素的质量比=39:127:(16×3)=39:127:48; (3)KIO3中碘(I)元素的质量分数= 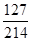 ×100%≈59.3% ×100%≈59.3%(4)根据含碘量为20mg/kg可知,1000g该食盐含I元素的质量为20mg,则每袋食盐最少含碘10mg, 设每袋该食盐含有碘酸钾的质量为xmg, 由I原子守恒可得, I~KIO3 127 214 10mg x 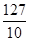 = =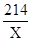 , ,解得x=16.9mg, 问题分析:利用图示中加碘盐的碘的含量可知500g该品牌食盐中,含碘的最大质量是 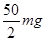 =25mg;因为一次性口服100毫克(不具放射性的碘原子),可使人体甲状腺中碘达到饱和,因该食盐的含碘量是50mg/kg,又因100毫克(不具放射性的碘原子),使人体甲状腺中碘达到饱和而不再吸收外界的碘,从而起到保护作用.所以需要至少食用2kg这种食盐才能达到碘的饱和; =25mg;因为一次性口服100毫克(不具放射性的碘原子),可使人体甲状腺中碘达到饱和,因该食盐的含碘量是50mg/kg,又因100毫克(不具放射性的碘原子),使人体甲状腺中碘达到饱和而不再吸收外界的碘,从而起到保护作用.所以需要至少食用2kg这种食盐才能达到碘的饱和;结论:因此日常食用这种食盐不会起到防辐射作用,因为每天食用食盐约为6g,远小于2Kg. 故答案为: [查阅资料(1)214 (2)K:I:O=39:127:48 (3)59.3% (4)KIO3的质量为:20mg÷59.3%≈33.7mg [问题分析2 Kg [结论①不能 ②因为每天食用食盐约为6g,远小于2㎏(其他合理答案也可) |
相似问题
油脂是重要的营养物质。油脂有人体内完全氧化时 每克放出约39.3kJ的能量。如果油脂的化学式为C57
油脂是重要的营养物质。油脂有人体内完全氧化时,每克放出约39 3kJ的能量。如果油脂的化学式为C57H110O6,则:(1)该油脂由_____________种元素组成,其
(5分) Fe2O3在一定条件下可转化为Fe0:Fe2O3+ C0高温2Fe0+C02 反应前Fe2
(5分) Fe2O3在一定条件下可转化为Fe0:Fe2O3+ C0高温2Fe0+C02,反应前Fe2O3的质量为160克,反应过程中,Fe2O3的转化率(参加反应的Fe2O3与反应前的Fe2O3
(5分)据报道:近年来在10多个城市的上万套全装修房项目中 大量使用甲醛严重超标 劣质的安信地板。我
(5分)据报道:近年来在10多个城市的上万套全装修房项目中,大量使用甲醛严重超标、劣质的安信地板。我国《室内装饰装修材料人造板及其制品中甲醛释放限
维生素C含片是保健食品 下图是XX牌维生素C含片的标签。请计算:(1) 维生素C的相对分子质量;(2
维生素C含片是保健食品,下图是XX牌维生素C含片的标签。请计算:(1) 维生素C的相对分子质量;(2) 维生素C中碳、氢、氧元素的质量比;(3) 维生素C中氧
学好化学可以避免生活中的盲目行为。日本大地震造成的核泄露事故使“防辐射”成为热点话题 “吃碘防辐射”
学好化学可以避免生活中的盲目行为。日本大地震造成的核泄露事故使“防辐射”成为热点话题,“吃碘防辐射”之说等原因在社会上造成短暂的“盐荒”。右表












