(5分) Fe2O3在一定条件下可转化为Fe0:Fe2O3+ C0高温2Fe0+C02 反应前Fe2
| (5分) Fe2O3在一定条件下可转化为Fe0:Fe2O3+ C0高温2Fe0+C02,反应前Fe2O3的质量为160克,反应过程中,Fe2O3的转化率(参加反应的Fe2O3与反应前的Fe2O3的质量比)用a表示,固体中铁元素与氧元素的质量比用mFe/m Fe0表示。 (1)填写下表中的空格:  (2)如果Fe2O3转让为Fe0的反应分两步进行:3 Fe2O3十C0高温2 Fe3O4十CO2 Fe304十3C0高温2FeO十CO2 反应后的固体中mFe/mO===21/8时固体的成分可能有三种情况: (1) Fe3O4 (2)▲ (填化学式、下同) (3)▲ . |
参考解答
| (1)FeO(1分) 50﹪(或0.5 2分) (2) Fe2O3和FeO(1分) Fe3O4、Fe2O3和FeO (1分位置可调换) |
| 分析:(1)根据Fe2O3的转化率是参加反应的Fe2O3与反应前的Fe2O3的质量比及固体中铁元素与氧元素的质量比,利用反应前Fe2O3的质量为160克代入化学反应方程式来解答; (2)根据反应后的固体中mFe/mO═21/8时,利用极限法来假设只生成氧化铁或氧化亚铁,先计算铁与氧元素的质量比再推测固体的成分. 解答:解:(1)根据Fe2O3+C0高温2Fe0+C02,Fe2O3的转化率是参加反应的Fe2O3与反应前的Fe2O3的质量比, 由表格中的转化率为100%可知,氧化铁全部反应, 则固体成分为FeO,氧化亚铁中Fe、O元素的质量比为56:16=7:2,符合题意; 当中mFe/mO═14/5时,设参加反应的氧化铁的质量为x, 则 Fe2O3+C0高温2Fe0+C02, 160 144 x 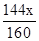 由反应后铁与氧元素的质量比得, 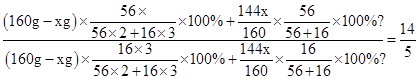 , ,解得x=80g, 则转化率为 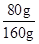 ×100%=50%, ×100%=50%,故答案为:FeO;50%; (2)由反应可知,反应后的固体有四氧化三铁、也可能有氧化亚铁, 若只有四氧化三铁,在Fe3O4中,铁、氧元素的质量比为56×3:16×4=21:8,则可能反应后固体只有四氧化三铁; 在Fe2O3中铁、氧元素的质量比为56×2:16×3=7:3=21:9, 若只有氧化亚铁,在FeO中Fe、O元素的质量比为56:16=7:2=21:6, 则7:3<21:8<Fe2O3<7:2, 则反应后固体可能为氧化铁和氧化亚铁的混合物,也可能为氧化铁、氧化亚铁、四氧化三铁的混合物, 故答案为:Fe2O3和FeO;Fe3O4、Fe2O3和FeO. 点评:本题计算较复杂,考查学生利用化学反应方程式及利用信息中转化率、元素质量比的计算,学生应充分利用信息并结合质量分数的概念、极限法、平均值法来综合应用解答本题. |
相似问题
(5分)据报道:近年来在10多个城市的上万套全装修房项目中 大量使用甲醛严重超标 劣质的安信地板。我
(5分)据报道:近年来在10多个城市的上万套全装修房项目中,大量使用甲醛严重超标、劣质的安信地板。我国《室内装饰装修材料人造板及其制品中甲醛释放限
维生素C含片是保健食品 下图是XX牌维生素C含片的标签。请计算:(1) 维生素C的相对分子质量;(2
维生素C含片是保健食品,下图是XX牌维生素C含片的标签。请计算:(1) 维生素C的相对分子质量;(2) 维生素C中碳、氢、氧元素的质量比;(3) 维生素C中氧
学好化学可以避免生活中的盲目行为。日本大地震造成的核泄露事故使“防辐射”成为热点话题 “吃碘防辐射”
学好化学可以避免生活中的盲目行为。日本大地震造成的核泄露事故使“防辐射”成为热点话题,“吃碘防辐射”之说等原因在社会上造成短暂的“盐荒”。右表
在由CH4和H2组成的混合气体中 测知碳元素的质量分数为60% 则混合气体充分燃烧生成二氧化碳和水的
在由CH4和H2组成的混合气体中,测知碳元素的质量分数为60%,则混合气体充分燃烧生成二氧化碳和水的质量比为 A.11∶18B.22∶9C.1∶1D.11∶27
人体缺钙易产生“骨质疏松症” 补钙保健品“盖中盖”钙片中的有效成分为碳酸钙[CaCO3] 试计算:(
人体缺钙易产生“骨质疏松症”,补钙保健品“盖中盖”钙片中的有效成分为碳酸钙[CaCO3],试计算:(1)碳酸钙的相对分子质量(2)计算:碳酸钙中Ca、C、O












