已知溶液中:还原性:-氧化性在含有3molNaHSO3的溶液中逐滴加入KIO3溶液 加入KIO3和析
已知溶液中:还原性: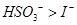 -氧化性 -氧化性 在含有3molNaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系如图所示,则下列说法错误的是( ) 在含有3molNaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系如图所示,则下列说法错误的是( )
|
参考解答
| C |
试题分析:依题意,该反应是按如下顺序进行的: 3HSO3-+IO3-=3SO42-+I-+3H+;(此处只能生成I-,因为还原性HSO3->I-) IO3-+5I-+6H+=3I2+3H2O A、此处只能是NaHSO3过量,正确;B、b点时还原产物还应该是碘离子,b点后就变为碘单质了,正确;C、b点到c点,KIO3与碘离子反应生成单质碘,错误;D、,正确。 |
相似问题
研究NO2 SO2 CO等大气污染气体的处理以及燃料的开发与利用有重要意义。(1)NO2可用水吸收
研究NO2、SO2、CO等大气污染气体的处理以及燃料的开发与利用有重要意义。(1)NO2可用水吸收,利用反应6NO2+8NH37N2+12H2O 也可以处理NO2。当转移1 2m
(12分)按图所示实验过程填空:(1)写出上述反应的离子方程式:①
(12分)按图所示实验过程填空:(1)写出上述反应的离子方程式:①②③(2)填空:ab cd
自然界地表层原生铜的硫化物经氧化 淋滤作用后变成CuSO4溶液 向地下深层渗透 遇到难溶的ZnS或P
自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下深层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜蓝(CuS)。下列分析正确的是A.CuS的
(1)将废钒催化剂(主要成分V2O5)与稀硫酸 亚硫酸钾溶液混合 充分反应 所得溶液显酸性 含VO2
(1)将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应,所得溶液显酸性,含VO2+、K+、SO42-等。写出该反应的化学方程式_____________
氮化铝(AlN)广泛应用于电子 陶瓷等工业等领域。在一定条件下 AlN可通过如下反应制取: 下列叙述
氮化铝(AlN)广泛应用于电子、陶瓷等工业等领域。在一定条件下,AlN可通过如下反应制取:,下列叙述正确的是 ( )A.AlN中氮的化合价为+3B.AlN的摩尔












