(6分)某反应池中 发生“生物硝化过程” 利用 如果不考虑反应过程中硝化细菌的增殖 其净反应如下式所
(6分)某反应池中,发生“生物硝化过程”,利用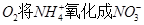 ,如果不考虑反应过程中硝化细菌的增殖,其净反应如下式所示: ,如果不考虑反应过程中硝化细菌的增殖,其净反应如下式所示: (1)完成上述反应的离子方程式并配平,将系数填入方框中(系数是1也要填)。 (2)将铵态氮中的1mg氮转化成硝酸根中的氮,需氧气 mg。(精确0.01) (3)取100mL完全反应后溶液,加入19.2g铜粉及一定量的稀硫酸,恰好完全反应(假设还原产物全部是NO气体),则原溶液中 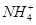 的浓度为 的浓度为 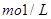 。(假设反应前后溶液的体积不变) 。(假设反应前后溶液的体积不变) |
参考解答
| (1)1,2;1,2,1 (2)4.57 (3) 2 |
| 此题综合考查了氧化还原方程式的配平及化学平衡的移动问题。在离子方程式的配平中既要遵守得失电子守恒,还要注意方程式两边电荷守恒。 (1)根据方程式可知,氮元素的化合价从-3价升高到+5价,失去8个电子。氧元素的化合价从0价降低到-2价,得到2个电子,所以根据电子的得失守恒可知,配平后的化学计量数依次是1,2;1,2,1。 (2)根据配平后的方程式可知,N~2O2,所以需要氧气是64mg÷14=4.57mg。 (3)19.2g铜粉的物质的量是0.3mol,失去0.6mol电子,所以生成0.2molNO,则氮原子总的物质的量是0.2mol,所以NH4+的浓度是0.2mol÷0.1L=2mol/L。 |
相似问题
(7分) 铜和浓硫酸发生反应的化学方程式为: Cu +2H2SO4(浓) CuSO4+SO2↑+2H
(7分) 铜和浓硫酸发生反应的化学方程式为: Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O(1)浓H2SO4作_________剂,具有性。(2)在该反应中,若消耗了32 g
硫酸铵在强热时分解的产物是二氧化硫.氮气.氨气.水 则该反应化合价变化和未变化的氮原子数之比为A.1
硫酸铵在强热时分解的产物是二氧化硫 氮气 氨气 水,则该反应化合价变化和未变化的氮原子数之比为A.1:4B.1:2C.2:1D.4:1
今年6月11日 我国“神十”载人航天飞船发射取得圆满成功。火箭发射时燃料燃烧的反应为:2 N2H4(
今年6月11日,我国“神十”载人航天飞船发射取得圆满成功。火箭发射时燃料燃烧的反应为:2 N2H4(g)+ 2NO2(g)= 3N2(g)+4H2O(l)△H=akJ mol, 关于此
(6分)已知一定质量的硫与100mL某浓度的KOH溶液恰好完全反应 其反应方程式为:3S+6KOH(
(6分)已知一定质量的硫与100mL某浓度的KOH溶液恰好完全反应,其反应方程式为:3S+6KOH(浓)= 2K2S+K2SO3+3H2O,若被还原的硫元素为1 6g。求该KOH溶液的物质的量的浓度。
试管壁上附着的硫可用CS2溶解清洗 也可倒入热的NaOH溶液将硫除掉 其反应方程式为3S+6NaOH
试管壁上附着的硫可用CS2溶解清洗,也可倒入热的NaOH溶液将硫除掉,其反应方程式为3S+6NaOH2Na2S+Na2SO3+3H2O。反应中氧化剂和还原剂的质量比为( )A












