在反应中:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O(1)______元素被还原;__
| 在反应中:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O (1)______元素被还原;______是氧化剂(填元素符号或化学式) (2)Cu发生了______反应;若某元素的化合价升高了,则该元素所在的生成物称为氧化产物,该反应的还原产物是______.(填元素符号或化学式) (3)用双线桥标出反应的电子转移方向和数目:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,若有1.5molCu发生了反应,则转移的电子的个数是______. |
参考解答
| (1)Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,反应中硫元素化合价从+6价变化为+4价,化合价降低做氧化剂,硫元素被还原, 故答案为:S;H2SO4; (2)氧化还原反应中铜元素化合价升高,失去电子做还原剂,被氧化为氧化产物;硫元素化合价降低,硫酸得到电子做氧化剂,被还原得到还原产物SO2, 故答案为:氧化;SO2; (3)氧化还原反应中,得电子的元素是硫,化合价降低2价,失电子的元素是铜,化合价升高2价,所以转移电子2mol;表示方法为: 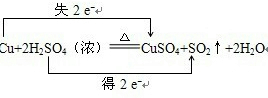 ; 若有1.5molCu发生了反应,依据电子转移故选计算:Cu~Cu2+~2e-;则转移的电子的个数是3NA; 故答案为:  ;3NA. |
相似问题
列说法正确的是( )①水玻璃 福尔马林 淀粉 Fe(OH)3胶体均为混合物③1H+ 2H2 3H互
列说法正确的是( )①水玻璃、福尔马林、淀粉、Fe(OH)3胶体均为混合物③1H+、2H2、3H互为同位素③用紫色石蕊试液检验HCHO溶液是否被氧化④酸化的Ba
实验室可用KMnO4和浓盐酸反应制取氯气.其变化可表述为:______KMnO4+______HCl
实验室可用KMnO4和浓盐酸反应制取氯气.其变化可表述为:______KMnO4+______HCl(浓)═______KCl+______MnCl2+______Cl2↑+______H2O(1)请配平化学方
必考题高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.(1)
必考题高锰酸钾是锰的重要化合物和常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.(1)KMnO4稀溶液是一种常用的消毒剂.其消毒机理与
二氧化硒(Se)是一种氧化剂 其被还原后的单质硒可能成为环境污染物 通过与浓HNO3或浓H2SO4反
二氧化硒(Se)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se.完成下列填空:(1)Se和浓HNO3反应
铁及其化合物在生活 生产中有广泛应用.请回答下列问题:(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的
铁及其化合物在生活、生产中有广泛应用.请回答下列问题:(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为:3FeS2+8O2高温 6SO2+Fe3












