课外活动小组的同学对学校附近的赤铁矿中Fe2O3含量进行测定.取样品20g加到309g盐酸中 恰好完
| 课外活动小组的同学对学校附近的赤铁矿中Fe2O3含量进行测定.取样品20g加到309g盐酸中,恰好完全反应后,经过滤、干燥、称重,得滤渣的质量为4g(杂质不与盐酸反应)。请计算: (1)赤铁矿中Fe2O3的质量分数。 (2)反应后所得滤液中溶质的质量分数。 |
参考解答
| (1)赤铁矿中Fe2O3的质量为:20g-4g=16g 赤铁矿中Fe2O3的质量分数: 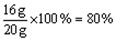 (2)设滤液中FeCl3的质量为x。 Fe2O3+6HCl==2FeCl3+3H2O 160 2×162.5 16g x 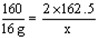 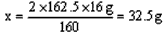 滤液中溶质的质量分数为: 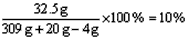 |
相似问题
现有5gCO与CO2的混合气体 将其通过足量灼热的CuO(假设反应完全进行) 测知反应后气体的质量比
现有5gCO与CO2的混合气体,将其通过足量灼热的CuO(假设反应完全进行),测知反应后气体的质量比原来增加了32%,原混合气体中CO、CO2的质量比为[ ]A 8:17B 11:14C 14:11D 14:111
黄铜是由铜和锌所组成的合金 用途广泛。某兴趣小组为探究黄铜合金的组成 取20.00g粉末状黄铜合金样
黄铜是由铜和锌所组成的合金,用途广泛。某兴趣小组为探究黄铜合金的组成,取20 00g粉末状黄铜合金样品,把60 00g稀硫酸平均分成三等份,分三次加入样品
某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数 取用16g石灰石样品 把80g稀盐酸(氯化氢
某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用16g石灰石样品,把80g稀盐酸(氯化氢的水溶液)分4次加入样品中(样品中除碳酸钙外,其余
将10g质量分数为20%的氢氧化钠溶液与20g质量分数为10%的硫酸溶液混合后 所得溶液不能与下列物
将10g质量分数为20%的氢氧化钠溶液与20g质量分数为10%的硫酸溶液混合后,所得溶液不能与下列物质发生反应的是 [ ]A.CuCl2 B.Na2CO3 C.CO2 D.Ba(NO3)2
48g镁 54g铝分别跟足量的稀硫酸反应 按上述反应顺序 得到氢气的质量比是___。
48g镁、54g铝分别跟足量的稀硫酸反应,按上述反应顺序,得到氢气的质量比是___。












