(8分)已知A B C D E五种元素的原子序数依次递增 A B C D位于前三周期。A位于周期表的
| (8分)已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子对数与未成对电子数之比为3:1。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1∶1的化合物N是常见的有机溶剂。E有“生物金属”之称,E4+和氩原子的核外电子排布相同。 (1)D元素在元素周期表中的位置为第 周期 族。 (2)下列叙述正确的是 (填写序号)。 a.水的沸点比M高得多,是因为水分子间能形成氢键,而M分子间不能形成氢键 b.M的中心原子采用sp3杂化 c.N分子中含有6个σ键和1个大π键 d.BD2晶体的熔点、沸点都比二氧化硅晶体的低 (3)已知C2D是一种麻醉剂,根据等电子原理可推知C2D的空间构型为 。 (4)E的一种氧化物Q,其晶胞结构如图所示,则Q的化学式为 。 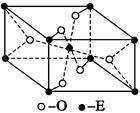 |
参考解答
| (1)二(1分)VIA(1分)(2)ad(2分,漏选得1分,错选倒扣分,本空不出现负分) (3)直线形(2分)(4)TiO2(2分) |
试题分析:A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同,短周期s区,只有ⅠA有单电子,则A为氢元素;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,则B原子电子排布式为1s22s22p2,故B为碳元素;D原子的核外成对电子对数与未成对电子数之比为3:2,A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,则D为O元素,M是甲醛,所以C为N元素;A、B两种元素组成的原子个数之比为1∶1的化合物N是常见的有机溶剂,则N是苯。E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同,则E的原子序数为18+4=22,为Ti元素,则 (1)氧元素在周期表中的位置是第二周期第ⅥA族。 (2)a.水的沸点比甲醛高得多,是因为水分子间能形成氢键,而M分子间不能形成氢键,a正确;b.甲醛是平面形结构,中心原子采用sp2杂化,b不正确;c.N分子中含有12个σ键和1个大π键,c不正确;d.CO2是分子晶体,二氧化硅是原子晶体,其熔点、沸点都比二氧化硅晶体的低,d正确,答案选ad。 (3)N2O与CO2互为等电子体,二氧化碳是直线形结构,则N2O也是直线形结构。 (4)由晶胞结构可知,晶胞中Ti元素数目为1+8× 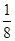 =2,O原子数目为2+4× =2,O原子数目为2+4×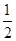 =4,故该氧化物的化学式为TiO2。 =4,故该氧化物的化学式为TiO2。 |
相似问题
镓(Ga) 锗(Ge) 砷(As) 硒(Se)均为第四周期的元素 它们在高科技尖端科学特别是信息领域
镓(Ga)、锗(Ge)、砷(As)、硒(Se)均为第四周期的元素,它们在高科技尖端科学特别是信息领域有着广泛的用途。试回答下列问题:(1)基态锗原子的价电子排布
已知大多数含氧酸可用通式XOm(OH)n来表示 如X是S 则m=2 n=2 则这个式子就表示H2SO
已知大多数含氧酸可用通式XOm(OH)n来表示,如X是S,则m=2,n=2,则这个式子就表示H2SO4。一般而言,该式中m大于等于2的是强酸,m为0的是弱酸。下列各含氧
(15分)【化学——选修3:物质结构与性质】Ⅰ.顺铂是美国教授B Rosenberg等人于1969年
(15分)【化学——选修3:物质结构与性质】Ⅰ.顺铂是美国教授B Rosenberg等人于1969年发现的第一种具有抗癌活性的金属配合物,它的化学式为Pt(NH3)2
能源 材料和信息是现代社会的三大“支柱”。(1)目前 利用金属或合金储氢的研究已取得很大进展 下图是
能源、材料和信息是现代社会的三大“支柱”。(1)目前,利用金属或合金储氢的研究已取得很大进展,下图是一种镍基合金储氢后的晶胞结构图。① Ni原子的价
A B C D E为原子序数依次增大的短周期元素 已知A B E 3种原子最外层共有11个电子 且这
A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和












