“神七”登天标志着我国的航天事业进入了新的篇章。(1)火箭升空时 由于与大气层的剧烈摩擦 产生高温。
| “神七”登天标志着我国的航天事业进入了新的篇章。 (1)火箭升空时,由于与大气层的剧烈摩擦,产生高温。为了防止火箭温度过高,在火箭一面涂上一种特殊的涂料,该涂料的性质最可能的是 。
该反应中被氧化的原子与被还原的原子的物质的量之比是 。这个反应应用于火箭推进器,除释放大量的热和快速产生大量气体外,还有一个很大的优点是 。 (3)如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,燃料电池放电时的负极反应为: 。如果某段时间内氢氧储罐中共收集到33.6L气体(已折算成标况),则该段时间内水电解系统中转移电子的物质的量为 mol。 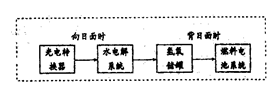 (4)在载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料。 已知该反应的阳极反应为:4OH—4e-=O2↑+2H2O 则阴极反应为: 。有人提出,可以设计反应2CO=2C+O2(△H>0、△S<0)来消除CO的污染。请你判断上述反应是否能发生? 理由 。 (5).北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。丙烷脱氢可得丙烯。 已知:①C3H8(g)  CH4(g)+HC≡CH(g)+H2(g); △H1="156.6" kJ·mol-1 CH4(g)+HC≡CH(g)+H2(g); △H1="156.6" kJ·mol-1②CH3CH=CH2(g)  CH4(g)+ HC≡CH (g);△H2="32.4" kJ·mol-1 CH4(g)+ HC≡CH (g);△H2="32.4" kJ·mol-1则相同条件下,反应C3H8(g)  CH3CH=CH2(g)+H2(g)的△H=_____kJ·mol-1 CH3CH=CH2(g)+H2(g)的△H=_____kJ·mol-1 |
参考解答
| (1)B (2)1 2 3 4 ;2:1 产物无污染(3)H2-2e-+2OH-=2H2O 2 (4)2CO2+4e-+2H2O=2CO+4OH- 不可行 △H>0,吸热 △S<0 (5)(124.2) |
试题分析:该涂料的性质最可能的是在高温下可分解气化。分解吸热,产物气化也消耗大量的能量,可以使火箭温度降低。选项为:B。(2)火箭升空需要产生高能的反应的方程式是1N2O4+2N2H4==3N2+4H2O。系数是1 2 3 4。该反应中被氧化N2H4中的N的原子与被还原的原子的N2O4中的N原子的物质的量之比是2:1. 这个反应应用于火箭推进器,除释放大量的热和快速产生大量气体外,还有一个很大的优点是产物无污染、洁净、环保。(3)在氢氧燃料电池中,通入H2的电极作负极,发生的电极反应为:H2-2e-+2OH-=2H2O. 2H2O------2H2↑+ O2↑。产生气体3mol,转移电子4mol.现在产生气体共1.5mol,所以转移电子2mol.(4)根据总反应式及阳极的电极反应式可得到阴极反应为:2CO2+4e-+2H2O=2CO+4OH- 有人设计2CO=2C+O2(△H>0、△S<0)来消除CO的污染的方案不可行。原因是该反应的△H>0,是吸热反应;△S<0,体系的混乱程度减小。(5)①-②整理得:C3H8(g)  CH3CH=CH2(g)+H2(g)的△H=124.2KJ/mol. CH3CH=CH2(g)+H2(g)的△H=124.2KJ/mol. |
相似问题
(14分)制烧碱所用盐水需两次精制。第一次精制主要是用沉淀法除去粗盐水中Ca2+ Mg2+ SO42
(14分)制烧碱所用盐水需两次精制。第一次精制主要是用沉淀法除去粗盐水中Ca2+、Mg2+、SO42-等离子,过程如下:Ⅰ 向粗盐水中加入过量BaCl2溶液,过
4 mL 0.5 mol/L的某KXO4溶液恰好能将160 mL 0.1 mol/L的FeSO4的酸
4 mL 0 5 mol L的某KXO4溶液恰好能将160 mL 0 1 mol L的FeSO4的酸性溶液反应完全,则X元素在还原产物中的化合价为A.-1B.0C.+2D.+3
高锰酸钾(KMnO4)是一种常用的氧化剂。(1)有下列变化:CO32-→CO2 C2O42-→CO2
高锰酸钾(KMnO4)是一种常用的氧化剂。(1)有下列变化:CO32-→CO2、C2O42-→CO2、Fe3+→Fe2+,找出其中一个变化与“MnO4-→Mn2+”组成一个反应,写
某离子反应中涉及H2O ClO— NH4+ H+ N2 Cl—六种微粒。其中N2的物质的量随时间变化
某离子反应中涉及H2O、ClO—、NH4+、H+、N2、Cl—六种微粒。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是:A.该反应的还原剂是Cl—B.
下列变化需要加入氧化剂才能实现的是( )A.HCl→H2B.NaCl→Cl2C.CuSO4→CuD
下列变化需要加入氧化剂才能实现的是( )A.HCl→H2B.NaCl→Cl2C.CuSO4→CuD.HClO→O2












