下图由短周期元素形成的物质之间的转化关系 其中A D L为单质 其他为化合物.其中化合物I J K中
下图由短周期元素形成的物质之间的转化关系,其中A、D、L为单质,其他为化合物.其中化合物I、J、K中含有两种相同的元素,G和I的反应⑤是一种重要化工生产中的主要反应之一.B常温下为液态化合物,F是一种直线型的非极性气体分子.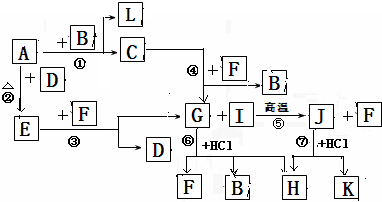 试回答下列有关问题: (1)以上7个化学反应属于自身氧化还原反应的是______ (用编号①→⑦填写) (2)在G、J、H中含有相同的元素是______; (3)J的水溶液和F______填写”能”或”否”)发生反应,其理由是______ (4)反应⑤的化学方程式是______. (5)写出电解溶液H的阴极电极反应方程式是______. |
参考解答
| “G和I的反应⑤是一种重要化工生产中的主要反应之一”.然后看G和盐酸反应的生成物,为三种,所以初步鉴定,G为弱酸含氧盐.生成物为,H为氯酸盐,因为B常温下为液态化合物,所以是水B为水,F为二氧化碳; G是碳酸钠,B是水,F是二氧化碳,I是二氧化硅,J是硅酸钠,H是两个反应的共同产物,故为NaCl,K为H2SiO3;依据转化关系,C为NaOH,A、D、L为单质,A和B反应生成氢氧化钠和L,则A为Na,L为H2,A和D反应生成E,E和F生成碳酸钠和D,推断为E为Na2O2,D为O2, (1)根据推断可知①是置换反应,②是化合反应,③是氧化还原反应,④是复分解反应,⑤是复分解反应,⑥是复分解反应,⑦是复分解反应,所以发生自身氧化还原反应的是过氧化钠和二氧化碳的反应为③,故答案为:③; (2)在G为Na2CO3、J为Na2SiO3、H为NaCl,所以三种物质中含有相同的元素是Na,故答案为:Na; (3)J(Na2SiO3)的水溶液和F(CO2)反应生成碳酸钠和硅酸,反应的理由是较强酸制较弱的酸,故答案为:能 较强酸制较弱的酸; (4)反应⑤是二氧化硅和碳酸钠在高温条件下反应生成硅酸钠和二氧化碳,反应的化学方程式是:SiO2+Na2CO3
(5)电解溶液H(NaCl)的阴极电极反应方程式是:2H2O+2e-=2OH-+H2↑;故答案为:2H2O+2e-=2OH-+H2↑. |
相似问题
过氧化钠(Na2O2)是中学常见物质 常见的过氧化物还包括过氧化钙(CaO2).已知:过氧化钠与CO
过氧化钠(Na2O2)是中学常见物质,常见的过氧化物还包括过氧化钙(CaO2).已知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成
MnO2+4HCl(浓)═MnCl2+Cl2+2H2O 中氧化剂______ 还原剂______ 氧
MnO2+4HCl(浓)═MnCl2+Cl2+2H2O中氧化剂______,还原剂______,氧化产物______,转移电子______.
新交通法规定酒驾一次扣12分.如图为交警对驾驶员是否饮酒进行检测.其原理如下:2CrO3(红色)+3
新交通法规定酒驾一次扣12分.如图为交警对驾驶员是否饮酒进行检测.其原理如下:2CrO3(红色)+3C2H5OH+3H2SO4=Cr2(SO4)3(绿色)+3CH3CHO+6H2O该反应
氧化剂MO(OH)2+中的M元素的化合价为+5 用25mL 0.028mol/L的Na2SO3溶液恰
氧化剂MO(OH)2+中的M元素的化合价为+5,用25mL0 028mol L的Na2SO3溶液恰好将含有2 8×10-4molMO(OH)2+的溶液还原,并生成SO42-,则M元素的最终价态是
国家质检总局调查结果显示:所谓毒奶粉是被三聚氰胺所污染 它可由三聚氰酸[C3N3(OH)3]制备.三
国家质检总局调查结果显示:所谓毒奶粉是被三聚氰胺所污染,它可由三聚氰酸[C3N3(OH)3]制备.三聚氰酸可用于消除汽车尾气中的NO2,已知三聚氰酸中氮元












