某学习小组同学用久置的过氧化氢溶液(如图)制取氧气 取2g二氧化锰于锥形瓶中 然后慢慢滴入34g过氧
某学习小组同学用久置的过氧化氢溶液(如图)制取氧气,取2g二氧化锰于锥形瓶中,然后慢慢滴入34g过氧化氢溶液,充分反应。完成下列分析及计算: ⑴小明根据过氧化氢中氧元素的质量分数计算氧气的质量,其计算式为: 生成氧气的质量=34g×10%××100% =34g×10%× 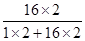 ×100%=3.2g。 ×100%=3.2g。老师指出小明的计算是错误的,你认为错误的原因是 ▲ (填字母序号)。 A.过氧化氢的氧元素的质量分数计算有误 B.过氧化氢中的氧元素没有全部转移到氧气中 ⑵请你根据化学方程式帮助小明计算理论上可制取氧气的质量。 ⑶小亮思考:过氧化氢不稳定会自然分解,导致溶液中溶质的质量分数减小。实验结束后,称得锥形瓶内剩余物质的总质量是35.2g。请计算这瓶过氧化氢溶液中实际溶质的质量分数。 |
参考解答
| (1)B (2)1.6g (3)O2=34g+2g—35.2g=0.8g H2O2%=5% |
| 分析:(1)根据过氧化氢生成氧气的生成物和 反应原理进行分析; (2)根据过氧化氢分解方程式中的等量关系进行分析解答; (3)根据氧气的量计算出过氧化氢的质量,计算质量分数; 解:(1)过氧化氢分解制取氧气时,生成了水和氧气,过氧化氢中的氧元素没有全部转化为氧气,有一部分在水中,故答案为:B; (2)解:设生成氧气质量为x, 2H2O2 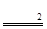 H2O+O2↑ H2O+O2↑68 32 34×10% x 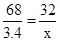 x=1.6g, 答:理论上可制取氧气的质量为:1.6g; (3)根据质量守恒定律可知,生成氧气质量为:O2=34g+2g-35.2g=0.8g 设需要过氧化氢为y, 2H2O2 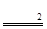 2H2O+O2↑ 2H2O+O2↑68 32 y 0.8g 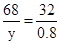 y=1.7g, 所以 H2O2%= 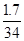 ×100%=5%, ×100%=5%,答:过氧化氢溶液中实际溶质的质量分数为5%. |
相似问题
某同学为了测定某石灰石中碳酸钙的质量分数(石灰石中的杂质不与盐酸反应).现取25g石灰石样品 加入足
某同学为了测定某石灰石中碳酸钙的质量分数(石灰石中的杂质不与盐酸反应).现取25g石灰石样品,加入足量的稀盐酸,同时测量5分钟内生成气体的质量,结
某环保小组监测到一工厂排放的废水中含有H2SO4和CuSO4.为了测定废水中CuSO4的质量分数 该
某环保小组监测到一工厂排放的废水中含有H2SO4和CuSO4.为了测定废水中CuSO4的质量分数,该小组取了100g废水,逐滴加入10%的NaOH溶液至过量.测得生成Cu
(6分)烧杯中装有一定量硫酸和硫酸铜的混合溶液 已知该溶液中含H2SO4的质量为9.8 g。某同学为
(6分)烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9 8 g。某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐(3)画出在该混
鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量 现取15g鸡蛋壳与80g稀盐酸
鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳与80g稀盐酸充分反应(蛋壳中的其他成分不溶于水,也不与稀盐酸反应)
4.6g某有机物在氧气中完全燃烧 生成8.8g二氧化碳和5.4g水 该有机物由______元素组成
4 6g某有机物在氧气中完全燃烧,生成8 8g二氧化碳和5 4g水,该有机物由______元素组成,该有机物中各元素原子的个数比为______.












