鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量 现取15g鸡蛋壳与80g稀盐酸
| 鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15g鸡蛋壳与80g稀盐酸充分反应(蛋壳中的其他成分不溶于水,也不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示。试计算: (1)产生CO2的质量为 g; (2)该鸡蛋壳中的CaCO3的质量分数。(写过程) 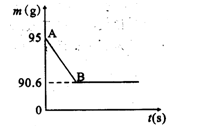 |
参考解答
| (1)4.4g (2)66.7% |
| 碳酸钙与盐酸反应放出二氧化碳使烧杯中的反应剩余物质量逐渐减小,根据质量守恒定律,完全反应前后的质量差即为反应放出气体二氧化碳的质量;根据生成二氧化碳的质量,利用反应的化学方程式及溶质的质量分数计算方法,即可求出参加反应的碳酸钙的质量,从而求出其质量分数.(1)反应生成CO2的质量为95g-90.6g=4.4g (2)设鸡蛋壳中含CaCO3的质量为x CaCO3+2HCl═CaCl2+H2O+CO2↑ 100 44 x 4.4g 100/x=44/4.4 解之得 x=10g 10/80×100%=66.7% |
相似问题
4.6g某有机物在氧气中完全燃烧 生成8.8g二氧化碳和5.4g水 该有机物由______元素组成
4 6g某有机物在氧气中完全燃烧,生成8 8g二氧化碳和5 4g水,该有机物由______元素组成,该有机物中各元素原子的个数比为______.
称取一定量的BaCl2的固体加水配成100g溶液 然后向该溶液中逐滴加入Na2SO4溶液 到反应终点
称取一定量的BaCl2的固体加水配成100g溶液,然后向该溶液中逐滴加入Na2SO4溶液,到反应终点(恰好完全反应)时消耗的Na2SO4溶液质量为100克,反应生成BaS
(6分)硅酸钠(Na2SiO3)是我国优先发展的精细化工产品 工业制备的反应为:2NaOH+ SiO
(6分)硅酸钠(Na2SiO3)是我国优先发展的精细化工产品,工业制备的反应为:2NaOH+ SiO2="=" Na2SiO3+ H2O 。现以125t石英砂(SiO2质量分数为96%)
在化合反应2A+B2==2AB中 A与B2反应的质量关系如右图所示 现将6gA和8g B2充分反应
在化合反应2A+B2==2AB中,A与B2反应的质量关系如右图所示,现将6gA和8g B2充分反应,则生成AB的质量是A.9gB.11gC.12gD.14g
(5分)有氯酸钾和二氧化锰的混合物共27.5 g 加热使之反应 待反应至不再有气体生成后 将试管冷却
(5分)有氯酸钾和二氧化锰的混合物共27.5 g,加热使之反应,待反应至不再有气体生成后,将试管冷却、称量,得到剩余固体17.9 g。求:⑴制取氧气的质












