(16分)粉煤灰 是从煤燃烧后的烟气中收捕下来的细灰 粉煤灰是燃煤电厂排出的主要固体废物。我国火电厂
(16分)粉煤灰,是从煤燃烧后的烟气中收捕下来的细灰,粉煤灰是燃煤电厂排出的主要固体废物。我国火电厂粉煤灰的主要氧化物为:SiO2、Al2O3,还含有FeO、Fe2O3等。现将提取粉煤灰中Al、Si等元素,某科研小组的同学设计了如下工艺流程: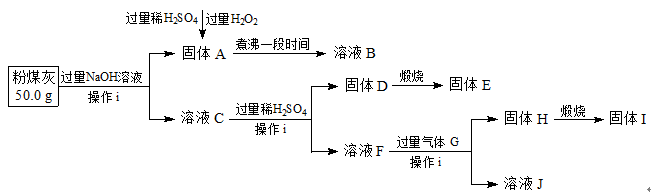 请回答下列问题: (1)操作i所需要的玻璃仪器有: (填序号)。 a.铁架台 b.烧杯 c.冷凝管 d.玻璃棒 e.集气瓶 f.分液漏斗 g.漏斗 (2)写出粉煤灰与过量NaOH溶液反应的离子方程式 。 (3)写出向固体A中加入过量稀H2SO4和过量H2O2时发生的离子反应方程式 。 (4)写出生成固体H的离子方程式 。 (5)该科研小组的同学准备用0.1 mol·L-1KSCN溶液和0.5000mol·L-1KI溶液滴定溶液B,以测定粉煤灰中Fe元素的含量: ①为减小实验误差,由固体A制备溶液B过程中煮沸的目的是 (请用化学方程式表示)。 ②判断滴定终点的现象为 。 ③将溶液B配制成250mL溶液后,取出25.00mL装入锥形瓶中,再滴入1~2滴KSCN溶液进行滴定,滴定过程中使用KI溶液的量如下表所示:
④若滴定操作太慢,则滴定结果 (填“偏小”、“偏大”或“无影响”);原因是 (请用离子方程式及简单的文字描述)。 |
参考解答
| (1)b、d、g(选对2个得1分,全对得2分)。 (2)SiO2+2OH-=SiO32-+H2O;Al2O3+2OH-=2AlO2-+H2O(各2分)。 (3)H2O2+2H++2Fe2+=2Fe3++2H2O(2分)。 (4)Al3++3NH3·H2O=Al(OH)3↓+3NH4+(2分)。 (5)①2H2O2=2H2O+O2↑(1分)。 ②溶液的血红色刚好退去,且半分钟内颜色无变化(2分)。 ③16.8%(2分)。 ④偏大(1分);滴定过慢,KI溶液被空气氧化,消耗KI溶液的体积增大,发生反应的离子方程式为:4H++4I-+O2=2I2+2H2O(2分)。 |
| (1)操作i是过滤,需要用到的玻璃仪器有:烧杯、玻璃棒、漏斗。 (2)粉煤灰中SiO2与Al2O3分别与过量NaOH溶液反应的离子方程式:SiO2+2OH-=SiO32-+H2O;Al2O3 +2OH-=2AlO2-+H2O。 (3)写出向固体A中加入过量稀H2SO4和过量H2O2的目的是将Fe2+氧化为Fe3+,发生反应的离子方程式为:H2O2+2H++2Fe2+=2Fe3++2H2O。 (4)固体H的主要成分Al2O3是溶液F中的Al3+与NH3反应生成的,其离子方程式为:Al3++3NH3·H2O=Al(OH)3↓+3NH4+。 (5)①加热煮沸的目的是让过量的H2O2完全分解,以防止干扰后面的滴定实验,化学方程式为:2H2O2=2H2O+O2↑。 ②以KSCN为指示剂,用标准KI溶液滴定未知的Fe3+,滴定终点的实验现象为:溶液的血红色刚好退去,且半分钟内颜色无变化。 ③由表可知,第二次滴定数据是错误的,不能用来算平均体积,故舍去。滴定消耗KI溶液的平均体积为30.00mL,根据: I- ~ Fe3+ 1mol 56g 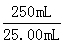 ×0.5000×30.00×10-3mol m(Fe3+) ×0.5000×30.00×10-3mol m(Fe3+)m(Fe3+)= 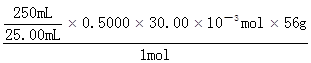 =8.40g =8.40g所以w(Fe)= 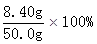 =16.8%。 =16.8%。④滴定过慢,KI溶液被空气氧化,消耗KI溶液的体积增大,故滴定结果偏大;发生反应的离子方程式为:4H++4I-+O2=2I2+2H2O。 本题来源于真实的化工工艺,废物中资源的回收、综合利用。该试题起点高、结构新颖,工业背景的题材多、提问灵活,该类题符合考纲“能够从试题提供的新信息中,准确地提取实质性内容,考查学生知识迁移的能力”。 将元素化合物知识放置在真实的化学工业环境中,从而达到考查同学们的综合分析问题的能力以及将新信息和已有信息整合,重组为新信息块的能力。是新课改区高考题的一大“亮点”。为必考题型之一。 |
相似问题
下列表示对应化学反应的离子方程式正确的是A.MnO2与浓盐酸反应制Cl2:MnO2+4HClMn2+
下列表示对应化学反应的离子方程式正确的是A.MnO2与浓盐酸反应制Cl2:MnO2+4HClMn2++2Cl-+Cl2↑+2H2OB.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3- +C
六种短周期元素 aA bB cC dD eE fF 已知原子序数大小关系是:a<e<c<b<f<d
六种短周期元素,aA、bB、cC、dD、eE、fF,已知原子序数大小关系是:a<e<c<b<f<d,且a+b=(c+d) 2;六种元素在周期表中的位置关系是:A、B同主族
(16分)石墨在材料领域有重要应用。某初级石墨中含SiO2(7.8%) Al2O3(5.1%) Fe
(16分)石墨在材料领域有重要应用。某初级石墨中含SiO2(7 8%)、Al2O3(5 1%)、Fe2O3(3 1%)和MgO(0 5%)等杂质。设计的提纯和综合应用工艺如下:(注:Si
下列反应的化学方程式或离子方程正确的是 A.CH3CH=CH2发生加聚反应:B.乙酸乙酯在酸性条件下
下列反应的化学方程式或离子方程正确的是A.CH3CH=CH2发生加聚反应:B.乙酸乙酯在酸性条件下水解:C.SO2通入到BaCl2溶液中:SO2+ Ba2++H2O= BaSO3↓+
物质M是一种日常生活中不可缺少的调味品。已知C可在D中燃烧发出苍白色火焰。M与其他物质的转化关系如下
物质M是一种日常生活中不可缺少的调味品。已知C可在D中燃烧发出苍白色火焰。M与其他物质的转化关系如下图所示(部分产物已略去):(1)写出用惰性电极电解












