海水是巨大的资源宝库。下图是人类从海水资源获取某些重要化工原料的流程示意图。回答下列问题:(1)操作
海水是巨大的资源宝库。下图是人类从海水资源获取某些重要化工原料的流程示意图。 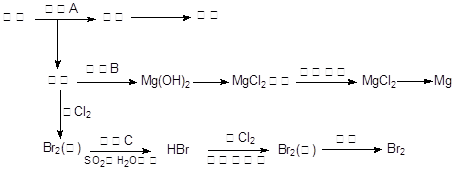 回答下列问题: (1)操作A是_________________(填实验基本操作名称)。用何种方法知道海水晒盐的过程中溶液里食盐含量在逐渐提高?________ a.分析氯化钠含量 b.测定溶液密度 c.观察是否有沉淀析出 (2)操作B需加入下列试剂中的一种,最合适的是______(选填编号)。 a.氢氧化钠溶液 b.澄清石灰水 c.石灰乳 d.碳酸钠溶液 (3)向苦卤中通入Cl2,发生反应的离子方程式是____________________________,操作C是_______________________________。 (4)上图中虚线框内流程的主要作用是_______________________;与之目的相同的流程在上图中还有几处,试指出其中一处________________________。 (5)将MgCl2转化为Mg时获得的副产品是_____________,用化学方程式表示该物质的某种用途______________________________________。 |
参考解答
| (1)蒸发结晶(1分),b(2分) (2)c;(1分) (3)Cl2 + 2Br- → Br2 + 2Cl-;(2分) 热空气吹出(1分) (4)富集Br2(1分);海水蒸发结晶得到粗盐、苦卤→Mg(OH)2→MgCl2溶液。(写出其中之一即可,1分) (5)Cl2;(1分) Cl2 + 2NaOH → NaCl + NaClO + H2O(其他合理答案均可)(2分) |
试题分析: (1)从海水中得到粗盐的操作应该是蒸发结晶。氯化钠的含量测定比较复杂,而观察法又不准确,所以最好的办法是测定溶液的密度,答案选b。 (2)向苦卤中加入石灰乳即可生成氢氧化镁沉淀,答案选c。 (3)冷却具有氧化性,能把溴离子氧化生成单质溴,反应的方程式是Cl2 + 2Br- → Br2 + 2Cl-;要使生成的单质溴溢出,则通过热空气吹出即可。 (4)上图中虚线框内流程的主要作用是富集单质溴。根据流程图可判断海水蒸发结晶得到粗盐、苦卤→Mg(OH)2→MgCl2溶液等均是富集单质溴的。 (5)电解熔融的氯化镁可以冶炼金属镁,同时得到氯气。在工业上氯气可以制备漂白液,反应的方程式是Cl2 + 2NaOH → NaCl + NaClO + H2O。 |
相似问题
鉴别下列各组物质 按要求回答问题。(1)稀硫酸 稀盐酸①可选作鉴别的试剂有(填编号 可多选)____
鉴别下列各组物质,按要求回答问题。(1)稀硫酸、稀盐酸①可选作鉴别的试剂有(填编号,可多选)_________。A.BaCl2溶液 B.Mg(NO3)2溶液 C.Na2CO3溶
下列各组物质的无色溶液 不用其他试剂即可鉴别的是( )①KOH Na2SO4 AlCl3②NaH
下列各组物质的无色溶液,不用其他试剂即可鉴别的是()①KOH Na2SO4 AlCl3②NaHCO3 Ba(OH)2 H2SO4③HCl NaAlO2 NaHSO4④Ca(OH)2 Na2CO3 BaCl2 A.①②B.②③C.①③④D.①②④
海洋约占地球表面积的71% 海水中化学资源的利用具有非常广阔的前景。(1)目前世界上60%的镁是从海
海洋约占地球表面积的71%,海水中化学资源的利用具有非常广阔的前景。(1)目前世界上60%的镁是从海水中提取的,其主要步骤如下:① 试剂①宜选用石灰乳
绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡 氧化铁等杂质
绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:已知:室温下饱和H2S
仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置(图2 图3)就能实现相应实验目的是
仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置(图2、图3)就能实现相应实验目的是












