在一个容积固定为2L的密闭容器中 发生反应△H=?。反应情况记录如下表:时间c(A)/mol L
在一个容积固定为2L的密闭容器中,发生反应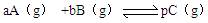 △H=?。反应情况记录如下表: △H=?。反应情况记录如下表:
(1)a2= ,b= ,p= 。(取最小正整数) (2)第2min到第4min内A的平均反应速率v(A)= mol·L-1·min-1[来源:学.科.网] (3)由表中数据可知反应在第4min到第6min时处于平衡状态,若在第2min、第6min、第8min时分别改变了某一反应条件,则改变的条件分别可能是: ①第2min 或 ②第6min ; ③第8min ; (4)若从开始到第4min建立平衡时反应放出的热量为235。92kJ,则该反应的△H= 。 |
参考解答
(1)1 2 2(3分) (2)0.2(2分) (3)①使用催化剂或升高温度(4分)②增加B的浓度(2分)③减小C的浓度(2分) (4) -196.6 kJ·mol-1(2分) |
略 |
相似问题
对达到平衡状态的可逆反应:X+Y W+Z 在t'时增大压强 则正逆反应速率变化如图所示(V代表速率
对达到平衡状态的可逆反应:X+Y W+Z,在t"时增大压强,则正逆反应速率变化如图所示(V代表速率,t代表时间)下列有关X、Y、Z、W的状态叙述正确的是A.X
(12分)373K时 某 1L密闭容器中加入1mol NH3发生如下可逆反应: 2NH3(g) N2
(12分)373K时,某 1L密闭容器中加入1mol NH3发生如下可逆反应: 2NH3(g) N2(g)+ 3 H2(g)。其中物质H2的物质的量变化如下图所示。(1)前
(15分)化学学科中的平衡理论主要包括:化学平衡 电离平衡 水解平衡和溶解平衡四种 且均符合勒夏特列
(15分)化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理。请回答下列问题:Ⅰ.有甲、乙两个容积相
一定温度下 将2mol A 2mol B 2mol C的气体混合物充入一体积不变密闭容器中 充分反应
一定温度下,将2mol A、2mol B、2mol C的气体混合物充入一体积不变密闭容器中,充分反应后恢复到起始温度,测得容器内的压强比起始时增大了20%,则容
下列事实中 不能用勒夏特列原理解释的是A.Fe(SCN)3溶液中加入固体KSCN后颜色变深B.向稀盐
下列事实中,不能用勒夏特列原理解释的是A.Fe(SCN)3溶液中加入固体KSCN后颜色变深B.向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低C.氢气、碘蒸气、


 L-1
L-1 in
in









