(12分)373K时 某 1L密闭容器中加入1mol NH3发生如下可逆反应: 2NH3(g) N2
(12分)373K时,某 1L密闭容器中加入1mol NH3发生如下可逆反应: 2NH3(g) N2(g)+ 3 H2(g)。其中物质H2的物质的量变化如下图所示。 N2(g)+ 3 H2(g)。其中物质H2的物质的量变化如下图所示。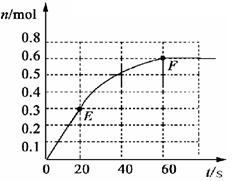 (1)前 20 s内NH3(g)的平均反应速率为  (2)373K时该反应的平衡常数的值为 (3)若在此平衡体系中再加入 1mol的NH3,与原平衡比较,新平衡时 NH3的转化率 (填“增大”或“减小”,下同)。NH3的平衡浓度 。 (4)将原平衡升温至 473K,重新达平衡时(其他条件不变),H2的平衡浓度为NH3的2倍,该反应的正反应为(填“放热反应”或 “吸热反应”) ,为增大平衡体系中H2的物质的量,下列措施正确的是(其它条件相同) a.升高温度 b.扩大容器的体积 c.加入合适的催化剂  d.再充入N2 d.再充入N2 |
参考解答
(1) 0.01mol/L·s (2) 0.12 (3)减小 增大 (4 )吸热 ab )吸热 ab |
| 略 |
相似问题
(15分)化学学科中的平衡理论主要包括:化学平衡 电离平衡 水解平衡和溶解平衡四种 且均符合勒夏特列
(15分)化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理。请回答下列问题:Ⅰ.有甲、乙两个容积相
一定温度下 将2mol A 2mol B 2mol C的气体混合物充入一体积不变密闭容器中 充分反应
一定温度下,将2mol A、2mol B、2mol C的气体混合物充入一体积不变密闭容器中,充分反应后恢复到起始温度,测得容器内的压强比起始时增大了20%,则容
下列事实中 不能用勒夏特列原理解释的是A.Fe(SCN)3溶液中加入固体KSCN后颜色变深B.向稀盐
下列事实中,不能用勒夏特列原理解释的是A.Fe(SCN)3溶液中加入固体KSCN后颜色变深B.向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低C.氢气、碘蒸气、
在密闭容器中有可逆反应:nA(g)+mB(g) pC(g) △H>0处于平衡状态(已知m+n>p)
在密闭容器中有可逆反应:nA(g)+mB(g)pC(g) △H>0处于平衡状态(已知m+n>p),则下列说法正确的是①升温,c(B) c(C)的比值变小②降温时体系内混合
(8分)在一定温度下的5L的密闭固定容积容器中 通入10molNH3 发生了如下反应:N2+3H22
(8分)在一定温度下的5L的密闭固定容积容器中,通入10molNH3,发生了如下反应:N2+3H22NH3,反应进行到2min时,测得容器内有2molN2,求:(1)2min时的












