(一)BaCl2·xH2O中结晶水数目可通过重量法来确定:①称取1.222g样品 置于小烧杯中 加入
| (一)BaCl2·xH2O中结晶水数目可通过重量法来确定: ①称取1.222g样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到沉淀完全,静置; ②过滤并洗涤沉淀; ③将盛有沉淀的滤纸包烘干并中温灼烧;转入高温炉中,反复灼烧到恒重,称得沉淀质量为1.165g。 回答下列问题: (1)在操作②中,需要先后用稀硫酸和 洗涤沉淀; (2)计算BaCl2·xH2O中的x= (取整数值)。 (3)操作③中,如果空气不充足和温度过高,可能会有部分沉淀被滤纸中的碳还原为BaS,这使x的测定结果 (填“偏低”、“偏高”或“不变”)。 (二)、(5分)图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞 如图B所示。且该物质为自然界最硬的物质。  回答下列问题: (1)图B对应的物质名称是 ,(2)d中元素的原子核外电子排布式为 。 (3)图A中由二种元素组成的物质中,沸点最高的是 , (4)图A中的双原子分子中,极性最大的分子是 。 (5)k的分子式为 , |
参考解答
| (一)(1)蒸馏水 取水洗液于试管中,加入稀硝酸酸化,滴加AgNO3溶液,若无白色浑浊出现,则表明Cl-已经冼净。 (2) 2 (3)偏高。 (二)(1)金刚石 (2)1s22s22p63s23p5 (3)H2O (4)HCl (5)COCl2 |
试题分析: (一)(1)洗涤必须用到蒸馏水 (2)样品中BaCl2的物质的量为 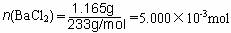 质量 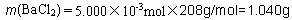 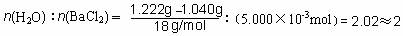 (3)题中已经表明硫酸钡被还原为BaS,则沉淀质量减小,相对水的质量比提高,x数据将偏高。 (二)(1)每个a原子周围有4个键,则图B对应的物质为金刚石;该晶胞中的原子数为:8× 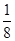 +6× +6×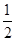 =4=8。 =4=8。(2)a为C,则b为H2、c为O2,因i是常见的酸,只由b、d形成可判断为盐酸,则d为Cl2。Cl原子核外有17个电子,其排布式为:1s22s22p63s23p5。 (3)除a、b、c、d外,f为CO,g为CO2,i为HCl,而k与水反应生成CO2与盐酸,判断K为COCl2。所有两元素形成的物质中,只有水是液态,其它都是气体;H2O中,中心原子O形成2条共价键、2对孤对电子,故O采取sp3杂化,形成V形分子。 (4)所有双原子分子中,只有H、Cl电负性差值最大,因而极性最大。(5)COCl2中C原子含有3个σ键,1个π键,故C原子采取sp2杂化。 |
相似问题
依据物质的相关数据 可以推断物质的结构和性质。下列利用物质的相关数据作出的相应推断不合理的是A.依据
依据物质的相关数据,可以推断物质的结构和性质。下列利用物质的相关数据作出的相应推断不合理的是A.依据元素的原子序数,推断该元素原子的核外电子数B
卤素化学丰富多彩 能形成卤化物 卤素互化物 多卤化物等多种类型的化合物。(1)卤素互化物如IBr I
卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。(1)卤素互化物如IBr ICl等与卤素单质结构相似、性质相近。Cl2、IBr、ICl沸
已知A B C D E都是周期表中前四周期的元素 它们的核电荷数A<B<C<D<E。其中A B C是
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC2的晶体为离子晶体,其阳离
芦笋中的天冬酰胺(结构如图)和微量元素硒 铬 锰等 具有提高身体免疫力的功效。(1)天冬酰胺所含元素
芦笋中的天冬酰胺(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。(1)天冬酰胺所含元素中,_______(填元素名称)元素基态原子核外未成
亚氨基锂(Li2NH)是一种储氢容量高 安全性好的固体储氢材料 其储氢原理可表示为:Li2NH+H2
亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:Li2NH+H2LiNH2+LiH,下列有关说法中正确的是 [ ]A Li2NH中N的化合价












