已知A B C D E都是周期表中前四周期的元素 它们的核电荷数A<B<C<D<E。其中A B C是
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC2的晶体为离子晶体,其阳离子与阴离子的个数比为1:1,D的二价阳离子比C的简单阴离子多一个电子层。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E原子序数为26.回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示).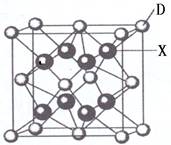 (1)E在周期表中的位置 (指明周期和族)。 (2)A、B、C的第一电离能由小到大的顺序为 . (3)B的氢化物的分子空间构型是 ;AC32-的中心原子采取 杂化. (4)写出任意一种由两种元素组成的与DC2中的阴离子互为等电子体的微粒的化学式 。 (5)E的高价态离子和低价态离子均能与A、B两元素按原子个数比1:1形成的带一个单位负电荷的阴离子组成六配位的配离子。写出该配离子的化学式 (任写一种). (6)X是周期表中电负性最大的元素,该元素与D元素组成的离子化合物的晶胞如右图所示。该离子化合物的化学式为 . |
参考解答
| (1)第四周期第Ⅷ族 (2)C<O<N (3)三角锥形 sp2 (4)IF、BrF、ClF、BrCl、Icl、Ibr、Cl0-等 (5)[Fe(CN)6]3-或者[Fe(CN)6]4-(6)CaF2 |
试题分析:由题给信息科推知A:C;B:N;C:O;D:Ca;E:Fe.(1)Fe时26号元素,它在元素周期表中的位置是第四周期第Ⅷ族。(2)C的核外电子排布是1s22s22p2;N的核外电子排布是1s22s22p3;O的核外电子排布是1s22s22p4.当原子核外的电子处于全充满或半充满或全空时是稳定的。的第一电离能由小到大的顺序为C<O<N。(3)NH3的分子空间构型是三角锥形。N在锥顶,三个H原子在锥底。CO32-的中心C原子采sp2杂化方式。(4)原子数相同,各原子最外层电子数之和相同的微粒互称为等电子体,它们也具有相似的结构特征。与C22-互为等电子体的微粒有IF、BrF、ClF、BrCl、Icl、Ibr、Cl0-等。(5)E的高价态离子和低价态离子均能与A、B两元素按原子个数比1:1形成的带一个单位负电荷的阴离子组成六配位的配离子是[Fe(CN)6]3-或者[Fe(CN)6]4-。(6)X是周期表中电负性最大的元素,X是F.该元素与D元素组成的离子化合物的晶胞如右图所示。Ca2+:8×1/8+6×1/2=4;F-:8×1=8.Ca2+:F-=4:8=1:2.所以该离子化合物的化学式为CaF2。 |
相似问题
芦笋中的天冬酰胺(结构如图)和微量元素硒 铬 锰等 具有提高身体免疫力的功效。(1)天冬酰胺所含元素
芦笋中的天冬酰胺(结构如图)和微量元素硒、铬、锰等,具有提高身体免疫力的功效。(1)天冬酰胺所含元素中,_______(填元素名称)元素基态原子核外未成
亚氨基锂(Li2NH)是一种储氢容量高 安全性好的固体储氢材料 其储氢原理可表示为:Li2NH+H2
亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:Li2NH+H2LiNH2+LiH,下列有关说法中正确的是 [ ]A Li2NH中N的化合价
碘具有升华的性质 利用该性质可用于指纹鉴定 因为A.汗液中有AgNO3 可以与碘生成黄色沉淀B.汗液
碘具有升华的性质,利用该性质可用于指纹鉴定,因为A.汗液中有AgNO3,可以与碘生成黄色沉淀B.汗液中有NaCl,可以与碘发生化学反应,有颜色变化C.根据
X Y Z和W代表原子序数依次增大的四种短周期主族元素 它们满足以下条件: ①X Y W分别位于不同
X、Y、Z和W代表原子序数依次增大的四种短周期主族元素,它们满足以下条件: ①X、Y、W分别位于不同周期;②在元素周期表中,Z与Y、W均相邻;③Y、Z、W三
(1)过渡金属元素铁能形成多种配合物 如:[Fe(H2NCONH2)6] (NO3)3[三硝酸六尿素
(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6] (NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等。① 基态Fe3+的M层电子排布式为。② 尿素(H2NC












