(1)写出Fe2(SO4)3在水溶液中的电离方程式:______(2)写出下列离子方程式对应的一个化
| (1)写出Fe2(SO4)3在水溶液中的电离方程式:______ (2)写出下列离子方程式对应的一个化学方程式:2H++CO32-=H2O+CO2↑______ (3)用“双线桥法”标明电子转移的方向和数目. MnO2+4HCl
该反应中氧化剂与还原剂物质的量之比为______ 该反应的离子方程式为______ (4)根据下列四个反应: ①Cl2+2KI=2KCl+I2 ②2FeCl2+Cl2=2FeCl3 ③2FeCl3+2HI=2FeCl2+2HCl+I2 ④H2S+I2=S+2HI 可以判断FeCl3、Cl2、I2、S四种物质的氧化性由强到弱的正确顺序是______. |
参考解答
| (1)Fe2(SO4)3在水溶液中的电离方程式为:Fe2(SO4)3=2Fe2++3SO42-,故答案为:Fe2(SO4)3=2Fe2++3SO42-; (2)2H++CO32-=H2O+CO2↑对应的化学反应为酸与碳酸氢盐的反应,化学方程式可写为HCl+NaHCO3-=H2O+NaCl+CO2↑,故答案为:HCl+NaHCO3-=H2O+NaCl+CO2↑; (3)MnO2+4HCl
Cl:-1升为0,失去1 mol电子,由于有2mol Cl化合价改变,所以共失去2mol电子,HCl是还原剂,氧化产物是Cl2,氧化剂和还原剂的物质的量之比为1:2,反应的离子方程式为MnO2+4H++2Cl-
电子转移的方向和数目 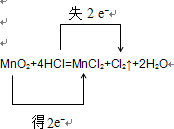 故答案为:  ;1:2;MnO2+4H++2Cl-
(4)①反应中Cl2>I2; ②反应中Cl2>FeCl3; ③反应中FeCl3>I2; ④反应中I2>S,所以氧化性顺序为Cl2>FeCl3>I2>S,故答案为:Cl2>FeCl3>I2>S. |
相似问题
下列化工生产过程中不涉及氧化还原反应的是( )A.氯碱工业B.硫酸工业C.玻璃工业D.合成氨工业
下列化工生产过程中不涉及氧化还原反应的是( )A.氯碱工业B.硫酸工业C.玻璃工业D.合成氨工业
人体正常血红蛋白中含有Fe2+ 若误食亚硝酸盐 会导致Fe2+转化为Fe3+而中毒 服用维生素C可以
人体正常血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化为Fe3+而中毒,服用维生素C可以解毒.对上述事实分析正确的是( )A.亚硝酸盐是还原剂B
氧化还原反应在生产 生活中用途广泛.下列事实中不涉及氧化还原反应的是( )A.金属的冶炼B.铁锅的
氧化还原反应在生产、生活中用途广泛.下列事实中不涉及氧化还原反应的是( )A.金属的冶炼B.铁锅的锈蚀C.石钟乳的形成D.食物的腐败
实验室可用KMnO4和浓盐酸反应制取氯气.其变化可表述为:______KMnO4+______HCl
实验室可用KMnO4和浓盐酸反应制取氯气.其变化可表述为:______KMnO4+______HCl(浓)═______KCl+______MnCl2+______Cl2↑+____________(1)请完成该化
当某金属变成相应的阳离子时 叙述正确的是( )A.得到电子被氧化B.失去电子被还原C.得到电子被还
当某金属变成相应的阳离子时,叙述正确的是( )A.得到电子被氧化B.失去电子被还原C.得到电子被还原D.失去电子被氧化












