某一反应体系中有反应物和生成物共五种物质:O2 H2CrO4 Cr(OH)3 H2O H2O2.已知
| 某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2. 已知该反应中H2O2只发生如下过程:H2O2-→O2. (1)该反应中的还原剂是______. (2)该反应中,发生还原反应的过程是______-→______. (3)写出该反应的化学方程式,并用单线桥法标出电子转移的方向和数目______. (4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为______. |
参考解答
| (1)由信息H2O2-→O2中可知,O元素的化合价由-1价升高到0,则H2O2为还原剂,故答案为:H2O2; (2)氧化剂发生还原反应,含元素化合价降低的物质为氧化剂,则Cr元素的化合价降低,即还原反应的过程为H2CrO4→Cr(OH)3,故答案为:H2CrO4;Cr(OH)3; (3)该反应中O元素失电子,Cr元素得到电子,2molH2CrO4反应转移电子为2mol×(6-3)=6mol,则用单线桥法标出电子转移的方向和数目为 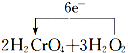 =2Cr(OH)3+3O2↑+2H2O,故答案为: 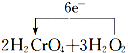 =2Cr(OH)3+3O2↑+2H2O; (4)由2H2CrO4+3H2O2═2Cr(OH)3+3O2↑+2H2O可知,生成3mol气体转移6mol电子,则转移了0.3mol电子,则产生的气体的物质的量为
其在标准状况下体积为0.15mol×22.4L/mol=3.36L,故答案为:3.36. |
相似问题
(1)写出Fe2(SO4)3在水溶液中的电离方程式:______(2)写出下列离子方程式对应的一个化
(1)写出Fe2(SO4)3在水溶液中的电离方程式:______(2)写出下列离子方程式对应的一个化学方程式:2H++CO32-=H2O+CO2↑______(3)用“双线桥法”标明
下列化工生产过程中不涉及氧化还原反应的是( )A.氯碱工业B.硫酸工业C.玻璃工业D.合成氨工业
下列化工生产过程中不涉及氧化还原反应的是( )A.氯碱工业B.硫酸工业C.玻璃工业D.合成氨工业
人体正常血红蛋白中含有Fe2+ 若误食亚硝酸盐 会导致Fe2+转化为Fe3+而中毒 服用维生素C可以
人体正常血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化为Fe3+而中毒,服用维生素C可以解毒.对上述事实分析正确的是( )A.亚硝酸盐是还原剂B
氧化还原反应在生产 生活中用途广泛.下列事实中不涉及氧化还原反应的是( )A.金属的冶炼B.铁锅的
氧化还原反应在生产、生活中用途广泛.下列事实中不涉及氧化还原反应的是( )A.金属的冶炼B.铁锅的锈蚀C.石钟乳的形成D.食物的腐败
实验室可用KMnO4和浓盐酸反应制取氯气.其变化可表述为:______KMnO4+______HCl
实验室可用KMnO4和浓盐酸反应制取氯气.其变化可表述为:______KMnO4+______HCl(浓)═______KCl+______MnCl2+______Cl2↑+____________(1)请完成该化












