(12分)某学习小组为证明并观察铜与稀HNO3反应的产物是NO 设计了如下图所示的实验装置。请你根据
(12分)某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置。请你根据他们的思路,回答有关的问题。 (一)实验仪器:大试管、玻璃导管、橡皮塞、烧杯、棉花、注射器。 (二)实验药品:铜丝、稀硝酸、碳酸钙颗粒、烧碱溶液。 (三)实验原理: 铜与稀硝酸反应的离子反应方程式 ① 。 (四)实验步骤: 1、按右图所示连接好装置,检验装置的 ② ; 2、向试管中加入一定量的固体药品(填化学式) ③ ,然后向试管中倒入过量的稀硝酸,并迅速塞紧带铜丝和导管的橡皮塞; 3、让试管中的反应进行一段时间后,用蘸有NaOH溶液的棉花团封住导管口; 4、将铜丝向下移动插入试管液体中,使之与稀硝酸反应; 5、把注射器的针孔插入试管口的橡皮塞中,缓慢向试管内推入空气。 (五)实验讨论: 1、实验步骤②的目的是(写出反应的离子方程式,结合文字说明) ④ ; 2、实验步骤⑤的目的是(写出反应的化学方程式,结合文字说明) ⑤ 。 (六)实验评价: 该装置的优点是(任写一个即可) ⑥ ; 有同学提出:增加右图所示装置,在步骤②完成后,当有明显现象再撤去该装置,并继续步骤③的“用蘸有NaOH溶液的棉花团封住导管口”。请评价他的做法 ⑦ 。 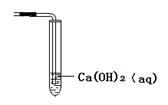 |
参考解答
| ① 3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO↑+ 4H2O(2分) ②气密性(1分) ③CaCO3(1分) ④ CaCO3 + 2H+ = Ca2+ + CO2↑+ H2O (2分),利用CO2排出试管中的空气,防止O2与NO反应(1分) ⑤ 2NO + O2 = 2NO2(1分),气体由无色变红棕色证明Cu与稀硝酸反应生成NO(1分) ⑥使用可抽动的铜丝能随时控制反应的开始和结束,节约药品用量,减少污染气体的产生。(或使用蘸有NaOH溶液的棉花团封住导管口,可防止NO和NO2气体逸出污染大气。)(2分) ⑦通过石灰水变浑浊的现象准确判断试管内无空气后,才进行步骤④,使得出的结论更科学。(1分) |
| ①硝酸是氧化性酸,能和铜发生氧化还原反应,方程式为3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO↑+ 4H2O。 ②制气装置连接好后,首先检验装置的气密性。 ③由于装置中含有空气,会氧化生成的NO,从而干扰实验,所以需要先排尽装置中的空气。可以利用硝酸和碳酸钙反应生成的CO2来实现,即加入的固体药品是碳酸钙,反应的方程式为CaCO3 + 2H+ = Ca2+ + CO2↑+ H2O。 ⑤由于NO极易被氧化生成红棕色NO2,所以目的是证明Cu与稀硝酸反应生成NO的,方程式为2NO + O2 = 2NO2。 ⑥评价实验可以从操作的难易程度、尾气的处理、实验现象等考虑。根据装置及实验过程可知,优点是使用可抽动的铜丝能随时控制反应的开始和结束,节约药品用量,减少污染气体的产生。(或使用蘸有NaOH溶液的棉花团封住导管口,可防止NO和NO2气体逸出污染大气。) ⑦由于在排空气时,无法判断是否完全排尽,所以通过石灰水变浑浊的现象,来准确判断试管内无空气后,才进行步骤④,使得出的结论更科学。 |
相似问题
某实验小组用下列装置进行乙醇催化氧化的实验。(1)实验过程中铜网出现黑色和红色交替的现象 请写出相应
某实验小组用下列装置进行乙醇催化氧化的实验。(1)实验过程中铜网出现黑色和红色交替的现象,请写出相应的化学方程式 、。在不断鼓入空气的情况下,熄
某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去)。(1)写出实验室制取氨气
某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去)。(1)写出实验室制取氨气的化学方程式: _____________________________。
已知在pH为4-5的环境中 Cu2+几乎不水解 而Fe3+几乎完全水解。某学生欲用电解纯净的CuSO
已知在pH为4-5的环境中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生欲用电解纯净的CuSO4溶液的方法,根据电极上析出铜的质量以及电极上产生气体的体积
某种催化剂为铁的氧化物。化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样
某种催化剂为铁的氧化物。化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后
下列实验操作都可能引起实验误差 其中说法正确的是( )A.常温下测定的气体摩尔体积大于22.4 L
下列实验操作都可能引起实验误差,其中说法正确的是( )A.常温下测定的气体摩尔体积大于22 4 L·mol-1B.100 mL 0 1 mol·L-1NaOH溶液和100 mL












