(11分) 能源短缺是人类面临的重大问题。甲醇是一种可再生能源 具有广泛的开发和应用前景。工业上一般
| (11分) 能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇: 反应I:CO2(g)+3H2(g) 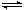 CH3OH(g)+H2O(g) CH3OH(g)+H2O(g)  ΔH1 ΔH1反应II:CO(g)+2H2(g) 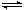 CH3OH(g) ΔH2 CH3OH(g) ΔH2(1)上述反应符合“原子经济”原则的是 (填“Ⅰ”或“Ⅱ”),反应I的化学平衡常数表达式K=  。 。(2)下表所列数据是反应Ⅱ在不同温度下的化学  平衡常数(K) 平衡常数(K)
②若容器容积不变,下列措施可增加甲醇产率的是 ; 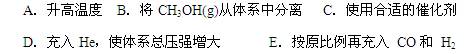 ③某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)="0.2" mol·L-1,则CO的转化率为 ,此时的温度为 (从上表中选择)。 |
参考解答
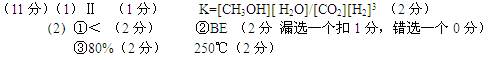 |
| 略 |
相似问题
体积相同的甲 乙两个容器中 分别充有2 mol SO2和1mol O2 在相同温度下发生反应2SO2
体积相同的甲、乙两个容器中,分别充有2 mol SO2和1mol O2,在相同温度下发生反应2SO2+O22SO3,并达到平衡.在该过程中,甲容器保持体积不变,乙容器
(16分)已知2A(g)+B(g)2C(g) △H=-a kJ/mol(a>0) 在一个有催化剂的固
(16分)已知2A(g)+B(g)2C(g),△H=-a kJ mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωm
反应:L(s)+aG(g)bR(g) 达到平衡时 温度和压强对该反应的影响如图所示:图中压强p1>p
反应:L(s)+aG(g)bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断( )
已知反应:2SO2(g)+O2(g) 2SO3(g) ΔH
已知反应:2SO2(g)+O2(g) 2SO3(g) ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强
(6分)一定条件下 向某容器中加入2molA 2molB 使反应2A+mBnC+D达到平衡时 气体A
(6分)一定条件下,向某容器中加入2molA、2molB,使反应2A+mBnC+D达到平衡时,气体A的浓度为w mol L、体积分数为v%。(1)若容积不变,且B为固体,达到












