(12分)“生物质'是指由植物或动物生命体衍生得到的物质的总称。“生物质能”是人类解决能源危机的一种
(12分)“生物质"是指由植物或动物生命体衍生得到的物质的总称。“生物质能”是人类解决能源危机的一种重要的能源。“生物质”在一定条件下可气化为CO、H2等原料气,进而合成甲醇和二甲醚(CH3OCH3),相关反应为: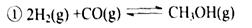  请根据图示回答问题: 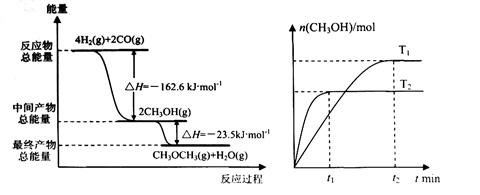 (1) 由H2和CO合成二甲醚的热化学方程式是 。 (2) 在T1、T2温度下,向两个容积相同的密闭容器中分别通入1molCO和2molH2合成甲醇,则T1、T2温度下对应反应的平衡常数K1_______K2(选填“<”、“>”或“=”)。 (3) 在一定条件下,向一个容积可变的密闭容器中充入4molH2、2molCO、1molCH3OCH3(g)和1molH20(g),经一定时间反应②达到平衡状态,此时测得混合气体密度是相同条件下起始时的1.6倍。反应开始时正、逆反应速率的大小关系为V(正)_______V(逆)(选填“ >”、“< ”或“=”),平衡时 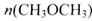 =_________mol。 =_________mol。(4) 右图为绿色电源“二甲醚燃料电池”的工作原理示意图。(a、b均为多孔性Pt电极) 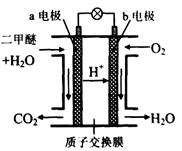 b电极是_______极:(填“正”或“负”) a电极上的电极反应为___ ____。 |
参考解答
(12分)(1) 4H2(g)+2CO(g)  CH3OCH3(g)+H2O(g) △H=-186.1 kJ/mol CH3OCH3(g)+H2O(g) △H=-186.1 kJ/mol(2) ﹥ (3) ﹥ ; 1.75(4)正 CH3OCH3 – 12e- +3H2O = 2CO2 + 12H+ |
试题分析:(1)根据图像可知,该反应的反应热△H=-162.6kJ/mol-23.5 kJ/mol=-186.1 kJ/mol,所以该反应的热化学方程式是4H2(g)+2CO(g)  CH3OCH3(g)+H2O(g) △H=-186.1 kJ/mol。 CH3OCH3(g)+H2O(g) △H=-186.1 kJ/mol。(2)根据图像可知T2曲线首先达到平衡状态,说明T2>T1。但温度越高,甲醇的物质的量越少,这说明升高温度,平衡向逆反应方向移动,即正反应是放热反应,所以K1>K2。 (3)根据方程式可知,该反应是体积减小的。由于气体的质量不变,所以如果平衡时混合气体密度是相同条件下起始时的1.6倍,就说明反应是向正反应方向进行的,因此反应开始时正、逆反应速率的大小关系为V(正) >V(逆)。 4H2(g)+2CO(g)  CH3OCH3(g)+H2O(g) CH3OCH3(g)+H2O(g)起始量(mol) 4 2 1 1 转化量(mol) 4x 2x x x 平衡量(mol)4-4x 2-2x 1+x 1+x 则 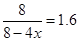 解得x=0.75mol 所以平衡时二甲醚的物质的量是1.75mol (4)氧气得到电子,在正极通入,所以b电极是正极;a电极是负极,二甲醚失去电子,由于存在质子交换膜,所以负极电极反应式是CH3OCH3-12e-+3H2O =2CO2+12H+。 点评:该题是高考中的常见题型,试题综合性强,难度较大。试题注重基础和能力的双向考查,有利于培养学生分析问题、解决问题的能力,也有助于培养学生的应试能力,提高学生的学习效率。 |
相似问题
对于铁在海水的腐蚀及防护设计实验如下(烧杯中装的是海水) 以下描述正确的是A.1中的铁被腐蚀得最快B
对于铁在海水的腐蚀及防护设计实验如下(烧杯中装的是海水),以下描述正确的是A.1中的铁被腐蚀得最快B.2中的铁被腐蚀得最慢C.3中是电化学防腐蚀的运
右图是模拟电化学反应装置图。下列说法正确的是( )A.若X为碳棒 开关K置于N处 会加快铁的腐蚀
右图是模拟电化学反应装置图。下列说法正确的是()A.若X为碳棒,开关K置于N处,会加快铁的腐蚀B.若X为锌,开关K置于N处,则X极上有黄绿色气体生成C.
钢铁发生吸氧腐蚀的时候 发生还原反应的电极方程式是A.Fe-2e-==Fe2+B.2H++2e-==
钢铁发生吸氧腐蚀的时候,发生还原反应的电极方程式是A.Fe-2e-==Fe2+B.2H++2e-==H2 ↑C.4OH--4e-==2H2O+O2↑D.2H2O+O2+4e-==4OH-
如图所示水槽中试管内有一枚铁钉 放置数天后观察:(1)铁钉在逐渐生锈 则铁钉的腐蚀属于_______
如图所示水槽中试管内有一枚铁钉,放置数天后观察:(1)铁钉在逐渐生锈,则铁钉的腐蚀属于________腐蚀。(2)若试管内液面上升,则原溶液呈________性,发
A B C三种强电解质 它们在水中电离出的离子如下表所示:阳离子Ag+ Na+阴离子NO3-
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:阳离子Ag+ Na+阴离子NO3- SO42- Cl-下图所示装置中,甲、乙、丙三个烧杯依次分别盛












