如图所示水槽中试管内有一枚铁钉 放置数天后观察:(1)铁钉在逐渐生锈 则铁钉的腐蚀属于_______
如图所示水槽中试管内有一枚铁钉,放置数天后观察: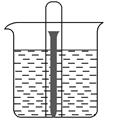 (1)铁钉在逐渐生锈,则铁钉的腐蚀属于________腐蚀。 (2)若试管内液面上升,则原溶液呈________性,发生________腐蚀,电极反应式为:负极:____________________,正极:____________________。 (3)若试管内液面下降,则原溶液呈________性,发生________腐蚀。电极反应式为,负极:____________________,正极:____________________。 |
参考解答
| (1)电化学 (2)弱酸性或中 吸氧 2Fe-4e-=2Fe2+ O2+2H2O+4e-=4OH- (3)较强的酸 析氢 Fe-2e-=Fe2+ 2H++2e-=H2↑ |
| 根据原电池的构成条件:有两种不同的材料(Fe为负极,碳为正极),有电解质溶液,形成闭合回路;可知铁钉的腐蚀属于电化学腐蚀。根据金属腐蚀的条件原理及结果可知:试管内液面上升,说明是试管内压强减小,试管内气体被吸收所致,是铁钉吸氧腐蚀的结果,据此写出电极反应式;试管内液面下降,说明是试管内气体压强变大,试管内产生了新气体所致,是铁钉析氢腐蚀的结果,据此写出电极反应式。 |
相似问题
A B C三种强电解质 它们在水中电离出的离子如下表所示:阳离子Ag+ Na+阴离子NO3-
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:阳离子Ag+ Na+阴离子NO3- SO42- Cl-下图所示装置中,甲、乙、丙三个烧杯依次分别盛
已知氧元素有16O 18O两种核素 按中学化学知识要求 下列说法正确的是 [ ]A.Na2O
已知氧元素有16O、18O两种核素,按中学化学知识要求,下列说法正确的是 [ ]A.Na2O2与H218O反应时生成产生18O2气体 B.向2SO2(g)+O2(g)2SO3(g)
关于如图所示各装置的叙述中 正确的是A.装置①是原电池 总反应是:Cu+2Fe3+=Cu2++2Fe
关于如图所示各装置的叙述中,正确的是A.装置①是原电池,总反应是:Cu+2Fe3+=Cu2++2Fe2+B.装置①中,铁作负极,电极反应式为:Fe3++e-=Fe2+C
钠硫高能蓄电池的结构如图 M为Na2O和Al2O3的混合物 电池的反应原理为电池工作温度为320℃。
钠硫高能蓄电池的结构如图,M为Na2O和Al2O3的混合物,电池的反应原理为电池工作温度为320℃。下列说法错误的是A.a为电池正极,b为电池负极B.电池放电时
电解水制取H2和O2时 为了增强溶液的导电性 常常要加入一些电解质 最好选用下列物质中的 [
电解水制取H2和O2时,为了增强溶液的导电性,常常要加入一些电解质,最好选用下列物质中的 [ ]A.HCl B.NaOH C.NaCl D.CuSO4












