根据下表回答问题.温度/℃020406080100溶解度(g/100g水)NaCl35.736.03
根据下表回答问题.
(2)60℃时在100g水中加入100g硝酸钾固体,充分溶解后所形成的溶液是______溶液(“饱和”或“不饱和”). (3)将上述(2)中溶液降温到20℃时,析出的晶体质量是______g. (4)工业上将硝酸钾和氯化钠的热混合溶液(两者均己达到饱和)冷却至室温,析出晶体. ①析出的晶体中主要物质是______; ②关于剩余溶液.下列说法正确的是______(填序号); A.只含氯化钠,不含硝酸钾 B.含有氯化钠,又含有硝酸钾,且只有硝酸钾达到饱和 C.含有氯化钠,又含有硝酸钾,且两者都达到饱和 (5)20℃时,将18克氯化钠溶解在80克水中,应至少蒸发______g水才能形成饱和溶液.蒸发时要用到玻璃棒,其作用是______. A.搅拌促进溶解B.加速蒸发 C.防止液滴飞溅D.引流缓冲 (6)如图为硝酸钾的溶解度曲线.M、N两点分别表示硝酸钾的两种溶液.下列做法能实现M、N间的相互转化的是______ A.从M→N:先将M升温再将其蒸发掉部分水 B.从M→N:先将M升温再将加入适量固体硝酸钾 C.从N→M:先将N降温再加入适量固体硝酸钾 D.从N→M:先过滤出适量固体硝酸钾再降温. 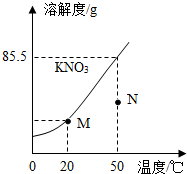 | |||||||||||||||||||||||
参考解答
| (1)40℃时,氯化钠固体的溶解度36.6g; (2)60℃时硝酸钠的溶解度110g,所以60℃时在100g水中加入100g硝酸钾固体,充分溶解后所形成的溶液是不饱和溶液; (3)20℃时硝酸钠的溶解度31.6g,所以将上述(2)中溶液降温到20℃时,析出的晶体质量是100g-31.6g=68.4g; (4)硝酸钾的溶解度受温度影响较大,①析出的晶体中主要物质是硝酸钾(KNO3);②剩余溶液含有氯化钠,又含有硝酸钾,且两者都达到饱和; (5)20℃时氯化钠固体的溶解度36.0g,所以20℃时,将18克氯化钠溶解在50克水中才能饱和,应至少蒸发30g水才能形成饱和溶液,蒸发时要用到玻璃棒,其作用是加速蒸发和防止液滴飞溅; (6)根据溶解度曲线的含义可知从M→N:先将M升温再将加入适量固体硝酸钾. 故答案为:(1)36.6;(2)不饱和;(3)68.4;(4)硝酸钾(KNO3);C;(5)30;BC;(6)B. |
相似问题
“食盐加碘”通常是在氯化钠中加入碘酸钾 是我国预防人民碘缺乏病最经济和最有效地措施.右图是氯化钠和碘
“食盐加碘”通常是在氯化钠中加入碘酸钾,是我国预防人民碘缺乏病最经济和最有效地措施.右图是氯化钠和碘酸钾的溶解度曲线图.下列说法错误的是(
如图 是a b两种物质(固体)的溶解度曲线 下列说法正确的是( )A.a的溶解度大于b的溶解度B.
如图,是a、b两种物质(固体)的溶解度曲线,下列说法正确的是( )A.a的溶解度大于b的溶解度B.a属于易溶物质,b属于难溶物质C.在t℃时,a、b两种
下图是a b两种物质的溶解度曲线.(1)t1℃时b的饱和溶液100g 恒温蒸发掉40g水后溶液的质量
下图是a、b两种物质的溶解度曲线.(1)t1℃时b的饱和溶液100g,恒温蒸发掉40g水后溶液的质量分数是______;(2)t2℃时a物质30g放入80g水中充分溶解溶液
如图是a b两种固体物质的溶解度曲线.下列说法中正确的是( )A.当温度小于t℃时 a的溶解度一定
如图是a、b两种固体物质的溶解度曲线.下列说法中正确的是( )A.当温度小于t℃时,a的溶解度一定比b小B.当温度大于t℃时,a溶液一定比b溶液浓C.t
出土木制文物常处于水饱和状态 出土后若任其自然干燥将收缩 变形.一种保持文物原状的方法是:将95份(
出土木制文物常处于水饱和状态,出土后若任其自然干燥将收缩、变形.一种保持文物原状的方法是:将95份(质量)K2SO4?A12(SO4)3?24H2O(明矾)和5份H2O












