(10分)某化学课外兴趣小组为探究铜跟浓硫酸的反应情况 用右图所示装置进行有关实验。请回答:(1)
| (10分)某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用右图所示装置进行有关实验。 请回答: 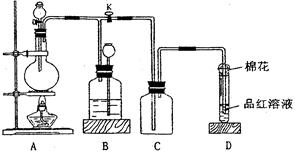 (1) 装置A中发生的化学反应方程式为 _____________________________________。 (2) 装置D中试管口放置的棉花中应浸一种液体,这种液体是 ,其作用是 。 (3) 装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是 。 B中应放置的液体是(填字母) 。 a.水 b.酸性KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液 (4) 实验中,取一定质量的铜片和一定体积18 mol·L—1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。 ① 有一定量的余酸但未能使铜片完全溶解,你认为原因是 。 ② 下列药品中能用来证明反应结束后的烧瓶中确有余酸的是________(填字母)。 a.NaOH固体 b.BaCl2溶液 c.银粉 d.Na2CO3溶液 |
参考解答
(10分)(1)Cu+2H2SO4(浓)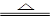 CuSO4+SO2↑+2H2O CuSO4+SO2↑+2H2O(2)碱液(其他合理答案均可给分); 吸收多余的二氧化硫,防止污染空气 (3)广口瓶中液面下降,而长颈漏斗中液面上升; d (4)①反应过程中浓硫酸被消耗,逐渐变稀,而铜不和稀硫酸反应 ②d |
试题分析:(1)本题探究铜跟浓硫酸的反应情况,由图可知,A为反应的发生装置,即铜与浓硫酸在加热的条件下发生反应; (2)装置D中试管口放置的棉花中应浸有可以吸收多余SO2的碱液,目的是防止污染空气; (3)装置B的作用是贮存多余的气体,B中应放置饱和NaHSO3溶液,故而B中现象是广口瓶中液面下降,而长颈漏斗中液面上升; (4)①反应过程中浓硫酸被消耗,逐渐变稀,而铜不和稀硫酸反应,故而不能反应完全,②用来检验是否还有硫酸,a.加入NaOH固体观察不到现象, b.加入BaCl2溶液只能证明硫酸根离子的存在,c.加入银粉不反应,d.加入Na2CO3溶液有气泡产生,现象明显,故选d 点评:本题考查铜与浓硫酸的反应,注意积累实验基础知识和环保理念,本题难度不大。 |
相似问题
某校研究性学习小组选择使用下列仪器和药品 验证由铜和适量浓硝酸反应产生的气体中含有NO(实验中使用的
某校研究性学习小组选择使用下列仪器和药品,验证由铜和适量浓硝酸反应产生的气体中含有NO(实验中使用的N2和O2的用量可自由控制)。已知:①NO + NO2
利用化学原理可以对工厂排放的废水 废渣等进行有效检测与合理处理。 (一)染料工业排放的废水中含有大量
利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。 (一)染料工业排放的废水中含有大量有毒的NO2-,可以在碱性条件下加入铝粉除去(
某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究。(1)提出假设:该反应的气体产物全部是
某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究。(1)提出假设:该反应的气体产物全部是二氧化碳。(2)设计方案:如图所示,将一定量
测定平衡常数对定量认识化学反应具有重要意义。已知:I2能与I-反应成I3- 并在溶液中建立如下平衡:
测定平衡常数对定量认识化学反应具有重要意义。已知:I2能与I-反应成I3-,并在溶液中建立如下平衡:I2 +I-I3-。通过测平衡体系中c(I2)、c(I-)和c(I3-),
工业上常用铁质容器盛装冷浓酸。为研究铁质材料与热浓硫酸的反应 某学习小组进行了以下探究活动[探究一]
工业上常用铁质容器盛装冷浓酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动[探究一] (1)将已去除表面氧化物的铁钉(碳素钢)放入












