反应3H2(g) + N2(g) 2NH3(g) ΔH = -46.19 kJ. mol—1 关
反应3H2(g) + N2(g)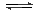 2NH3(g) ΔH = -46.19 kJ. mol—1,关于这个反应的平衡常数K,下列说法正确的是( ) 2NH3(g) ΔH = -46.19 kJ. mol—1,关于这个反应的平衡常数K,下列说法正确的是( )
|
参考解答
| C |
| 反应的平衡常数K,只与温度有关系,与压强无关,故B、D错误,升温,平衡左移,平衡常数K减小,故选C。 |
相似问题
由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙醇的技术流程:吸收池中盛有饱和碳
由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙醇的技术流程:吸收池中盛有饱和碳酸钾溶液,把含有二氧化碳的空气吹入吸收池中
(15分)甲醇是一种非常好的燃料。熔点-97.8°C 沸点64.5°C。一定条件下 CO与H2反应可
(15分)甲醇是一种非常好的燃料。熔点-97 8°C,沸点64 5°C。一定条件下,CO与H2反应可制得甲醇:CO+2H2CH3OH图1表示该反应进行过程中的能量变化;图2
可逆反应:N2 (g)+3H2 (g)2NH3(g)正反应放热 下列说法错误的是A.使用催化剂可加快
可逆反应:N2 (g)+3H2 (g)2NH3(g)正反应放热,下列说法错误的是A.使用催化剂可加快速率,提高生产效率B.N2不可能完全转化为NH3C.增大H2浓度可提高N2
现代工业将煤炭气化 既可以提高燃料的利用率 减少CO SO2等的排放 又可以扩大水煤气的广泛用途。⑴
现代工业将煤炭气化,既可以提高燃料的利用率、减少CO、SO2等的排放,又可以扩大水煤气的广泛用途。⑴已知:2C(s)+O2(g)=2CO(g);ΔH1 , 2H2(g)+O2(g)
已知: 某温度下的平衡常数为400。此温度下 在1 L的密闭容器中加人CH3OH 反应到某时刻测得
已知:,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加人CH3OH,反应到某时刻测得各组分的物质的量浓度如下:下列说法正确的是A 平衡后升












