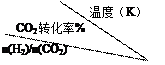由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙醇的技术流程:吸收池中盛有饱和碳
由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙醇的技术流程: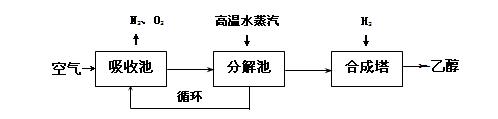 吸收池中盛有饱和碳酸钾溶液,把含有二氧化碳的空气吹入吸收池中,吸收池中反应液进入分解池后,向分解池中通入高温水蒸汽,把二氧化碳从溶液中提取出来,在合成塔中和氢气经化学反应使之变为可再生燃料乙醇。回答下列问题: (1)写出吸收池中反应的离子方程式 。 (2)从分解池中循环使用的物质是 。 (3)工业上还采取以CO和H2为原料合成乙醇,其化学反应方程式为: 2CO(g)+4H2(g) 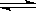 CH3CH2OH(g)+H2O(g) CH3CH2OH(g)+H2O(g)写出该反应的化学平衡常数表达式 K= 。 (4)在相同条件下,由CO制取CH3CH2OH的平衡常数远远大于由CO2制取CH3CH2OH的平衡常数。则由CO制取CH3CH2OH的优点是使原料有较大的转化率 ,由CO2制取CH3CH2OH的优点是 。(写出一点即可)
根据表中数据分析: ①温度升高,该反应的平衡常数K值 (选填“增大”、“减小”或“不变”); ②提高氢碳n(H2)/n(CO2)比,对生成乙醇 (选填“不利”、“有利”或“无影响”)。 |
参考解答
| (1)CO2+CO32-+H2O==2HCO3- (3分) (2)K2CO3 (3分) (3) 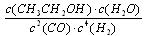 (3分) (3分)(4)CO2原料易得等 (3分)(其它合理答案均可给分) (5)①减小 (2分) ②有利 (2分) |
| 略 |
相似问题
(15分)甲醇是一种非常好的燃料。熔点-97.8°C 沸点64.5°C。一定条件下 CO与H2反应可
(15分)甲醇是一种非常好的燃料。熔点-97 8°C,沸点64 5°C。一定条件下,CO与H2反应可制得甲醇:CO+2H2CH3OH图1表示该反应进行过程中的能量变化;图2
可逆反应:N2 (g)+3H2 (g)2NH3(g)正反应放热 下列说法错误的是A.使用催化剂可加快
可逆反应:N2 (g)+3H2 (g)2NH3(g)正反应放热,下列说法错误的是A.使用催化剂可加快速率,提高生产效率B.N2不可能完全转化为NH3C.增大H2浓度可提高N2
现代工业将煤炭气化 既可以提高燃料的利用率 减少CO SO2等的排放 又可以扩大水煤气的广泛用途。⑴
现代工业将煤炭气化,既可以提高燃料的利用率、减少CO、SO2等的排放,又可以扩大水煤气的广泛用途。⑴已知:2C(s)+O2(g)=2CO(g);ΔH1 , 2H2(g)+O2(g)
已知: 某温度下的平衡常数为400。此温度下 在1 L的密闭容器中加人CH3OH 反应到某时刻测得
已知:,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加人CH3OH,反应到某时刻测得各组分的物质的量浓度如下:下列说法正确的是A 平衡后升
氮及其化合物在工农业生产 生活中有着重要作用。请回答下列问题:(1)右图是N2和H2反应生成2mol
氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:(1)右图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量