W X Y Z是四种常见的短周期主族元素 其原子半径随原子序数的变化如图所示。已知Y Z两种元素的单
W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。下列说法正确的是( )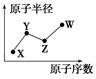
|
参考解答
| B |
| 首先推断出W、X、Y、Z依次是Cl、H、N、O。Cl、N的最简单氢化物分别是HCl。NH3,后者的水溶液呈碱性,A选项错误。H、N、O中任意两种都可以形成两种或两种以上的化合物,如NH3和N2H4,H2O和H2O2,N2O、NO和NO2等,B选项正确。H、N、O可形成NH4NO3,NH4+水解促进水的电离,C选项错误。Cl2不能从H2O中置换出O2,而是发生反应生成HCl和HClO,D选项错误。 |
相似问题
对于元素周期表 下列叙述中不正确的是( )A.在金属元素与非金属元素的分界线附近可以寻找制备
对于元素周期表, 下列叙述中不正确的是()A.在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素B.在过渡元素中可以寻找制备催化剂及耐
已知短周期元素甲 乙 丙 丁 戊的原子序数依次增大 其氢化物中甲 乙 丙 丁 戊的化合价如下 下列说
已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲、乙、丙、丁、戊的化合价如下,下列说法不正确的是元素甲乙丙丁戊化合价-3-2+1-
已知元素X Y的核电荷数分别是a和b 它们的离子Xm +和Yn - 的核外电子排布相同 则下列关系式
已知元素X、Y的核电荷数分别是a和b,它们的离子Xm +和Yn - 的核外电子排布相同,则下列关系式正确的是( )A.a = b+m+nB.a = b-m+nC.a = b+m-nD.a=b-m-n
元素的性质呈周期性变化的根本原因是( )A.元素的原子半径呈周期性变化B.元素原子量的递增
元素的性质呈周期性变化的根本原因是( )A.元素的原子半径呈周期性变化B.元素原子量的递增,量变引起质变C.元素的金属性和非金属性呈周期性变化D.元
短周期元素A B C D E的原子序数依次增大 A元素阳离子的原子核外没有电子 B是空气中含量最多的
短周期元素A、B、C、D、E的原子序数依次增大,A元素阳离子的原子核外没有电子,B是空气中含量最多的元素;C元素原子最外层电子数是其电子层数的三倍;C与












