钛和钛的合金已被广泛用于制造电讯器材 人造骨骼 化工设备 飞机等航天航空材料 被誉为“未来世界的金属
| 钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”。试回答下列问题: (1)钛有  和 和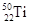 两种原子,它们互称为 ,钛基态原子的电子排布式为 ; 两种原子,它们互称为 ,钛基态原子的电子排布式为 ;(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构如图所示,它的化学式是 ; 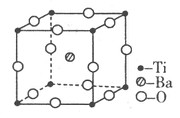 (3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如下: 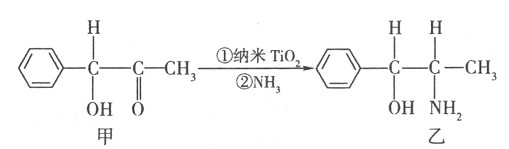 化合物甲的分子中采取sp2杂化的碳原子个数为 ,化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为 。 (4)现有含Ti3+的配合物,化学式为[TiCl(H2O)5]Cl2·H2O。配离子[TiCl(H2O)5] 2+ 中含有的化学键类型是 ,该配合物的配体是 。 |
参考解答
| (1)同位素(1分)1s22s22p63s23p63d24s2(1分) (2)TiBaO3(2分) (3)7(2分) N>O>C(2分) (4)极性键(或共价键)、配位键;(2分)H2O、Cl-(2分) |
试题分析:(1)质子数相同而中子数不同的原子,故为同位素;钛核外电子数为22,根据核外电子的排布原则可得电子排布式。(2)氧原子处于棱上,被四个这样的晶胞所共用,故12×1/4=3,钛原子位于顶点上,被8个这样的小立方体所共用,故8×1/8=1,钡原子位于立方体的中心,完全属于这个晶胞,根据三者的原子个数比可得化学式。(3)苯环上的碳原子均采取sp2杂化,碳氧双键中的碳原子也是sp2杂化,故7个;化合物乙中的碳原子、氮原子、氧原子均采取sp3杂化,氮原子外层p能级上是半充满结构,稳定,难失去电子,故第一电离能比氧原子大。(4)配离子[TiCl(H2O)5 2+中水分子中有极性键,Ti3+和氯原子及水分子均形成配位键,故配体为氯原子和水分子。 |
相似问题
现在V W X Y Z五种元素 它们的核电荷数依次增大 且都小于20 其中V的一种原子的原子核内没有
现在V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20,其中V的一种原子的原子核内没有中子;W和Y元素原子的最外层电子数相同,且W元素原子L
已知G Q X Y Z均为氯的含氧化合物。我们不了解它们的化学式 但知道它们在一定条件下具有下列转化
已知G、Q、X、Y、Z均为氯的含氧化合物。我们不了解它们的化学式,但知道它们在一定条件下具有下列转化关系(未配平) 这五种化合物中氯的化合价由低到高
J L M R T是原子序数依次增大的短周期主族元素 J R在周期表中的相对位置如右表;J元素最低负
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含
C N O是中学化学常见的三种元素 请回答下列问题:(1)写出基态O2-的核外电子排布式______
C、N、O是中学化学常见的三种元素,请回答下列问题:(1)写出基态O2-的核外电子排布式______________________________。(2)C、N、O三种元素的第一电离
[化学—选修3:物质结构与性质](15分)有A B C D E F G H原子序数递增的前四周期八种
[化学—选修3:物质结构与性质](15分)有A、B、C、D、E、F、G、H原子序数递增的前四周期八种元素。请根据下列信息,回答问题:①A、B、C、D、E、F为短周












