某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液。现有一瓶标签已破损的过氧化氢溶液 为测定瓶内
| 某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液。现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g。 请根据要求回答下列问题: (1)加入二氧化锰后发生反应的化学方程式为__________________________。 (2)生成氧气的质量是____。 (3)根据氧气的质量列出求解过氧化氢质量(x)的比例式_______________。 (4)瓶内过氧化氢溶液中溶质的质量分数是_____。 (5)若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液100g,需加入水的质量是____。 |
参考解答
(1)2H2O2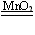 2H2O+O2↑ 2H2O+O2↑(2)3.2g (3)68/32=x/3.2g (4)20% (5)85g |
相似问题
在化学反应3H2+Fe2O32Fe+3H2O中 反应中各物质间的质量比为[ ]A.1∶1 B
在化学反应3H2+Fe2O32Fe+3H2O中,反应中各物质间的质量比为[ ]A 1∶1 B 3∶1∶2∶3C 3∶80∶56∶27D 1∶80∶28∶9
实验室常用一定质量分数的过氧化氢溶液制取氧气。某同学取2g二氧化锰于锥形瓶中 然后慢慢滴入34g过氧
实验室常用一定质量分数的过氧化氢溶液制取氧气。某同学取2g二氧化锰于锥形瓶中,然后慢慢滴入34g过氧化氢溶液,完全反应后,称得锥形瓶内剩余物质的总质
一瓶氢氧化钠固体 因不慎敞口放置了一段时间 已经部分变质。化学课外兴趣小组的同学决定测定该瓶试剂变质
一瓶氢氧化钠固体,因不慎敞口放置了一段时间,已经部分变质。化学课外兴趣小组的同学决定测定该瓶试剂变质的程度,他们在知识回顾的基础上,依次进行了
12.5g不纯的碳酸钙与足量的盐酸反应 生成4.4g二氧化碳 这种碳酸钙的纯度是(杂质不与盐酸反 应
12 5g不纯的碳酸钙与足量的盐酸反应,生成4 4g二氧化碳,这种碳酸钙的纯度是(杂质不与盐酸反 应)[ ]A.80%B.75%C.100%D.90%
实验室用6.5g锌与100g稀硫酸反应 当恰好完全反应时 求:(1)可制得氢气的质量是多少?(2)该
实验室用6 5g锌与100g稀硫酸反应,当恰好完全反应时,求:(1)可制得氢气的质量是多少?(2)该硫酸溶液的溶质质量分数。












