(15分)短周期元素X Y Z W在周期表中的位置如图所示 其中W的氧化物是酸雨形成的主要物质。(1
| (15分) 短周期元素X、Y、Z、W在周期表中的位置如图所示,其中W的氧化物是酸雨形成的主要物质。 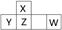 (1) 写出W的原子结构示意图: 。 (2) 将足量X的最高价氧化物通入含Y元素的阴离子溶液中。反应的离子方程式为 。 (3) 已知:①X(s) + O2(g) =XO2(g) ΔH=-393.5 kJ·mol-1 ②H2(g) + 1/2 O2(g) =H2O(g) ΔH=-242.0 kJ·mol-1 ③XH4(g) + 2O2(g) =XO2(g) + 2H2O(g) ΔH=-802.0 kJ·mol-1 则XH4气体分解成氢气和X固体的热化学方程式为 。 (4) ZO是由单质X和ZO2反应制取单质Z的中间产物。隔绝空气时,ZO与NaOH溶液反应(产物含有一种固体单质和一种钠盐)的化学方程式为_______________。 (5) 利用原电池原理,可用W的一种氧化物、O2和H2O来制备W的最高价氧化物对应水化物。写出该电池负极反应式:___________。 (6) 将W的气态氢化物通入一定量的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,生成气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。 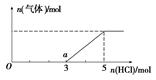 ①O点溶液中所含溶质的化学式为____________。 ②a点溶液中,c(Na+): c(Cl-)= _______________。 |
参考解答
(1)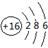 (2)AlO2-+ CO2 +2H2O = Al(OH)3↓+ HCO3- (2)AlO2-+ CO2 +2H2O = Al(OH)3↓+ HCO3-(3)CH4(g) =C (s) + 2H2(g);ΔH =+75.5 kJ·mol-1 (4)2SiO+ 2NaOH  Na2SiO3 + Si + H2O Na2SiO3 + Si + H2O (5)SO2 -2e-+ 2H2O = SO42-+ 4H+ (6)①Na2S、NaOH ②5 : 3 |
试题分析:根据题意可知这几种元素分别是:X是C;Y是Al;Z是Si;W是S。(1) S的原子结构示意图为 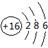 (2) 将足量CO2的最高价氧化物通入含AlO2-溶液中的反应的离子方程式为AlO2-+ CO2 +2H2O = Al(OH)3↓+ HCO3-.③-①-②×2整理可得CH4(g) =C (s) + 2H2(g);ΔH =+75.5 kJ·mol-1(4) ZO与NaOH溶液反应(产物含有一种固体单质和一种钠盐)的化学方程式为2SiO+ 2NaOH (2) 将足量CO2的最高价氧化物通入含AlO2-溶液中的反应的离子方程式为AlO2-+ CO2 +2H2O = Al(OH)3↓+ HCO3-.③-①-②×2整理可得CH4(g) =C (s) + 2H2(g);ΔH =+75.5 kJ·mol-1(4) ZO与NaOH溶液反应(产物含有一种固体单质和一种钠盐)的化学方程式为2SiO+ 2NaOH  Na2SiO3 + Si + H2O(5) 利用原电池原理,可用W的一种氧化物、O2和H2O来制备W的最高价氧化物对应水化物。该反应的总方程式为2SO2+O2+2H2O=2H2SO4,,该电池负极反应式为SO2 -2e-+ 2H2O = SO42-+ 4H+ 。(6)①在NaOH的溶液中通入H2S,发生的反应:2NaOH+H2S=Na2S+2H2O.若二者恰好反应。则滴加HCl时应该是Na2S+HCl='NaCl+NaHS;' NaHS+HCl=NaCl+H2S↑.前后的盐酸消耗的体积相同。但是由于在开始产生气体时消耗HCl的体积为3,当气体达到最大值时体积为5,说明原固体中含有NaOH和Na2S。即O点溶液中所含溶质的化学式为NaOH和Na2S。②在O点溶液中所含溶质的化学式为NaOH和Na2S,当滴加HCl至完全反应时,根据元素守恒可得n(Na+)= n(Cl-)= 5;而在a至恰好反应还需要HCl的物质的量为2mol,因此在a点时溶液中的n(Cl-)=3.因此在a点溶液中,c(Na+): c(Cl-)= 5 : 3。 Na2SiO3 + Si + H2O(5) 利用原电池原理,可用W的一种氧化物、O2和H2O来制备W的最高价氧化物对应水化物。该反应的总方程式为2SO2+O2+2H2O=2H2SO4,,该电池负极反应式为SO2 -2e-+ 2H2O = SO42-+ 4H+ 。(6)①在NaOH的溶液中通入H2S,发生的反应:2NaOH+H2S=Na2S+2H2O.若二者恰好反应。则滴加HCl时应该是Na2S+HCl='NaCl+NaHS;' NaHS+HCl=NaCl+H2S↑.前后的盐酸消耗的体积相同。但是由于在开始产生气体时消耗HCl的体积为3,当气体达到最大值时体积为5,说明原固体中含有NaOH和Na2S。即O点溶液中所含溶质的化学式为NaOH和Na2S。②在O点溶液中所含溶质的化学式为NaOH和Na2S,当滴加HCl至完全反应时,根据元素守恒可得n(Na+)= n(Cl-)= 5;而在a至恰好反应还需要HCl的物质的量为2mol,因此在a点时溶液中的n(Cl-)=3.因此在a点溶液中,c(Na+): c(Cl-)= 5 : 3。 |
相似问题
W M X Y Z是周期表前36号元素中的四种常见元素 其原子序数依次增大。W的一种核素在考古时常用
W、M、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质
下列比较错误的是A.原子半径:N>O>FB.酸性强弱:HNO3>H3PO4>H2SO4C.碱性强弱:
下列比较错误的是A.原子半径:N>O>FB.酸性强弱:HNO3>H3PO4>H2SO4C.碱性强弱:KOH >NaOH>Mg(OH)2D.氢化物的稳定性:HF>HCl>H2S
A B C D E F六种元素 其中A B C D E为短周期主族元素。它们之间的关系如下:(Ⅰ)原
A、B、C、D、E、F六种元素,其中A、B、C、D、E为短周期主族元素。它们之间的关系如下:(Ⅰ)原子半径:A < C < B < E < D(Ⅱ)原子的最外
液化石油气中常存在少量有毒气体羰基硫(COS) 必须将其脱除以减少环境污染和设备腐蚀。完成下列填空。
液化石油气中常存在少量有毒气体羰基硫(COS),必须将其脱除以减少环境污染和设备腐蚀。完成下列填空。(1)写出羰基硫的电子式,羰基硫分子属于(选填“
下列有关物质性质的比较 正确的是A.热稳定性:HF<HCl<HBrB.微粒半径: O2->Mg2+>
下列有关物质性质的比较,正确的是A.热稳定性:HF<HCl<HBrB.微粒半径: O2->Mg2+>Cl-C.第一电离能:Si>Al>MgD.电负性:Si>Al>Mg












