液化石油气中常存在少量有毒气体羰基硫(COS) 必须将其脱除以减少环境污染和设备腐蚀。完成下列填空。
| 液化石油气中常存在少量有毒气体羰基硫(COS),必须将其脱除以减少环境污染和设备腐蚀。完成下列填空。 (1)写出羰基硫的电子式 ,羰基硫分子属于 (选填“极性”、“非极性”)分子。 (2)下列能说明碳与硫两元素非金属性相对强弱的是 。 a.相同条件下水溶液的pH:Na2CO3>Na2SO4 b.酸性:H2SO3>H2CO3 c.CS2中碳元素为+4价,硫元素为-2价 (3)羰基硫在水存在时会缓慢水解生成H2S,对钢铁设备产生电化学腐蚀。写出正极的电极反应式 ,负极的反应产物为 (填化学式)。 为除去羰基硫,工业上常采用催化加氢转化法,把羰基硫转化为H2S再除去:COS + H2  CO + H2S CO + H2S (4)已知升高温度,会降低羰基硫的转化率。则升高温度,平衡常数K ,反应速率 (均选填“增大”、“减小”、“不变”)。 (5)若反应在恒容绝热密闭容器中进行,能说明该反应已达到平衡状态的是 。 a.容器内气体密度保持不变 b.容器内温度保持不变 c.c(H2)=c(H2S) d.υ(H2)正=υ(H2S)正 (6)已知该反应的平衡常数很大,说明 。 |
参考解答
(1)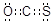 , 极性 (各1分,共2分) , 极性 (各1分,共2分)(2)a c (2分) (3)H2S + 2e → H2↑+S2-(或2H+ + 2e → H2↑)(2分) FeS(1分) (4)减小,增大(各1分,共2分) (5)b (2分) (6)正反应进行程度很大(1分。其他合理答案也给分) |
试题分析:(1)羰基硫相当于是二氧化碳中的1个氧原子被硫原子取代,所以其电子式为 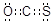 。S和O的非金属性不同,所以该化合物是极性分子。 。S和O的非金属性不同,所以该化合物是极性分子。(2)a.非金属性越强,最高价氧化物对应水化物的酸性越强,相应的钠盐水解程度越小,所以相同条件下水溶液的pH:Na2CO3>Na2SO4可以碳与硫两元素非金属性相对强弱,a正确;b.非金属性越强,最高价氧化物对应水化物的酸性越强,亚硫酸不是最高价含氧酸,所以酸性:H2SO3>H2CO3不能说明碳与硫两元素非金属性相对强弱,b不正确;c.CS2中碳元素为+4价,硫元素为-2价,说明非金属性是硫强于碳,c正确,答案选ac。 (3)原电池中负极失去电子发生氧化反应,正极得到电子发生还原反应,硫化氢分子中氢元素得到电子,发生还原反应,因此电极反应式为H2S + 2e → H2↑+S2-。负极铁失去电子,生成亚铁离子与硫离子结合生成硫化亚铁,所以负极产物是FeS。 (4)升高温度,会降低羰基硫的转化率,这说明升高温度平衡向逆反应方向移动,因此正方应是放热反应。则升高温度,平衡常数K减小,而反应速率增大。 (5)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,则a.密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,因此容器内气体密度始终保持不变,不能说明反应达到平衡状态,a不正确;b.由于反应在恒容绝热密闭容器中进行,所以容器内温度保持不变可以说明反应达到平衡状态,b正确;c.平衡时浓度不再发生变化,但物质的浓度之间不一定相等,故c(H2)=c(H2S) 不能说明反应达到平衡状态,c不正确;d.υ(H2)正=υ(H2S)正,但二者的反应速率方向相同,所以不能说明反应达到平衡状态,d不正确,答案选b。 (6)平衡常数越大,反应物的转化率越大,因此若该反应的平衡常数很大,说明正反应进行程度很大。 |
相似问题
下列有关物质性质的比较 正确的是A.热稳定性:HF<HCl<HBrB.微粒半径: O2->Mg2+>
下列有关物质性质的比较,正确的是A.热稳定性:HF<HCl<HBrB.微粒半径: O2->Mg2+>Cl-C.第一电离能:Si>Al>MgD.电负性:Si>Al>Mg
某元素X 它的原子最外层电子数是次外层电子数的2倍 则X在周期表中位于( )。A.第二周期B.第三
某元素X,它的原子最外层电子数是次外层电子数的2倍,则X在周期表中位于( )。A.第二周期B.第三周期C.第ⅣA族D.第ⅥA族
钾(K)与Na在性质上具有很大的相似性 但K比Na的活泼性强 下面是根据Na的性质对K的性质的预测
钾(K)与Na在性质上具有很大的相似性,但K比Na的活泼性强,下面是根据Na的性质对K的性质的预测,其中正确的是( )A.K是银白色金属,硬度大,熔点高B.K
下列微粒半径大小比较正确的是:A.Na+<Mg2+<Al3+<O2-B.S2->Cl->Na+>Al
下列微粒半径大小比较正确的是:A.Na+<Mg2+<Al3+<O2-B.S2->Cl->Na+>Al3+C.Na<Mg<Al<SD.Ca<Rb<K<Na
已知1~18号元素的离子aW3+ bX+ cY2— dZ—都具有相同的电子层结构 下列关系正确的是(
已知1~18号元素的离子aW3+、bX+、cY2—、dZ—都具有相同的电子层结构,下列关系正确的是()A.质子数:c>dB.离子的还原性:Y2—>Z —C.氢化物的稳












