有A B C D四种元素 A元素形成的离子中只有一个质子 B原子的最外层电子数是次外层的3倍 C元素
| 有A、B、C、D四种元素,A元素形成的离子中只有一个质子,B原子的最外层电子数是次外层的3倍,C元素的一价阳离子核外有10个电子,D元素的原子得到一个电子后能形成与氩原子电子层结构相同的离子.回答下列列问题: (1)画出D元素的离子结构示意图______; (2)工业上用电解C和D两元素形成的化合物的水溶液生产D的单质,写出该反应的化学方程式______,电解后的溶液能使酚酞变红的是与电源的______极相连接的区域; (3)D单质能和A、B、C三元素形成的化合物反应,该反应的化学方程式是______,当有0.1mol的D单质反应时,电子转移______个; (4)B、C、D三元素能形成一种化合物,1mol该化合物中有36mol电子,该化合物的水溶液是一种______剂,它与A、D两元素形成的化合物的水溶液反应时能产生一种有毒气体,该反应的化学方程式是______. |
参考解答
| 有A、B、C、D四种元素,A元素形成的离子中只有一个质子,则A是H元素,B原子的最外层电子数是次外层的3倍,则B元素是O元素,C元素的一价阳离子核外有10个电子,则C是Na元素,D元素的原子得到一个电子后能形成与氩原子电子层结构相同的离子,则D是Cl元素, (1)氯离子核外有3个电子层,最外层有8个电子,所以其离子结构示意图为: 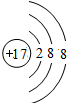 ,故答案为: ,故答案为: ; ;(2)电解氯化钠溶液生成氢氧化钠、氯气和氢气,电解方程式为:2NaCl+2H2O
故答案为:2NaCl+2H2O
(3)氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,反应方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,当有0.1mol氯气反应时,转移电子的个数=0.1mol×(1-0)NA=0.1NA, 故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;0.1NA; (4)B、C、D三元素能形成一种化合物,1mol该化合物中有36mol电子,该化合物是次氯酸钠,次氯酸钠具有强氧化性能杀菌消毒,所以次氯酸钠的水溶液是一种 消毒剂,次氯酸钠具有强氧化性,盐酸具有还原性,所以二者能发生氧化还原反应生成氯气,反应方程式为:NaClO+2HCl=NaCl+Cl2↑+H2O, 故答案为:消毒;NaClO+2HCl=NaCl+Cl2+H2O. |
相似问题
a.b.c.d.e是同周期的五种元素 a和b的最高价氧化物的水化物显碱性 且碱性b>a c和d的气态
a.b.c.d.e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且碱性b>a,c和d的气态氢化物的还原性d>c,五种元素的原子,得失电子后所形成的
A B C D E F六种短周期元素 其原子序数依次增大 在所有元素中A的原子半径最小 B原子最外层
A、B、C、D、E、F六种短周期元素,其原子序数依次增大,在所有元素中A的原子半径最小,B原子最外层电子数是次外层的2倍.A、E同主族,D、F同主族,且D、F
根据原子结构和元素周期律 回答:116号元素处于周期表第______周期 第______族;原子核外
根据原子结构和元素周期律,回答:116号元素处于周期表第______周期,第______族;原子核外有______个电子层,最外层有______个电子;它是______(填金属
X Y Z M N K是由短周期元素构成的微粒 其中X Y Z是阳离子 M N是中性分子 K是阴离子
X、Y、Z、M、N、K是由短周期元素构成的微粒,其中X、Y、Z是阳离子,M、N是中性分子,K是阴离子,它们具有下列结构特点和性质:①它们核外电子总数都相同
有关元素A B C D E F的信息如下:元 素有关信息A最高价氧化物对应的水化物(甲)能与其气态氢
有关元素A、B、C、D、E、F的信息如下:元素有关信息A最高价氧化物对应的水化物(甲)能与其气态氢化物(乙)反应生成盐B最外层电子数是次外层电子数的2倍












