(共12分)在容积固定为2L的密闭容器中 充入0.180 molHI 480℃时反应:2HI(g)H
| (共12分)在容积固定为2L的密闭容器中,充入0.180 molHI,480℃时反应: 2HI(g) 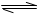 H2(g)+I2(g),体系中n(HI)随时间变化情况如下表: H2(g)+I2(g),体系中n(HI)随时间变化情况如下表:
(1)0~2min内H2的平均反应速度为 。达平衡时,HI的转化率是_________。(2)上述正向反应是: 反应(选填:放热、吸热)。 (3)某温度下上述反应平衡时,恒容、升高温度,原化学平衡向 反应方向移动(填“正”或“逆”),正反应速率 (填“增大”、“减小”或“不变”),容器内混合气体的压强 (填“增大”、“减小”或“不变”)。 (4)480℃时,反应H2(g)+I2(g) 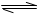 2HI(g)的平衡常数K的值为 。 2HI(g)的平衡常数K的值为 。(5)要增大反应2HI(g) 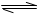 H2(g)+I2(g)的平衡常数,可采取的措施是 (选填字母)。 H2(g)+I2(g)的平衡常数,可采取的措施是 (选填字母)。A.增大HI起始浓度 B.向混合气体中通入I2 C.使用高效催化剂 D.升高温度 |
参考解答
| (1)0.002mol/(L·min),22.2% (2)吸热 (3)正,增大,增大。 (4)1/49 5)D |
(1)0~2min内HI的速率为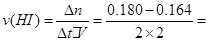 0.004mol/(L·min),由各物质的系数比可推出, 0.004mol/(L·min),由各物质的系数比可推出,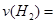 0.002mol/(L·min); 0.002mol/(L·min);由表格中数据可知,反应到8分钟时,HI的浓度不再改变,即反应已经达到平衡,此时HI的转化率为 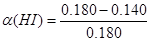 =22.2% =22.2%(2)由题意知,可逆反应2HI(g)  H2(g)+I2(g)降温时碘蒸气浓度减小,平衡左移,正反应为吸热反应 H2(g)+I2(g)降温时碘蒸气浓度减小,平衡左移,正反应为吸热反应(3)升温时,平衡向吸热反应方向移动,即正向移动;正逆反应速率均增大;由于两边气体系数相等,混合气体的总物质的量并不改变,但温度升高,由PV=nRT可知,压强增大 (4)由平衡常数的定义可知,在480℃时,K= 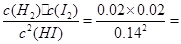 1/49 1/49(5)K只与温度有关,升温平衡右移,K增大,故答案为D |
相似问题
(8分)汽车尾气主要含有CO2 CO SO2 NO及汽油 柴油等物质 这种尾气越来越成为城市空气污染
(8分)汽车尾气主要含有CO2、CO、SO2、NO及汽油、柴油等物质,这种尾气越来越成为城市空气污染的主要来源,必须予以治理。治理的方法之一是在汽车的排气
(14分)氮可形成多种氧化物 如NO NO2 N2O4等 NO2和N2O4可以相互转化。(1)对反应
(14分)氮可形成多种氧化物,如NO、NO2、N2O4等,NO2和N2O4可以相互转化。(1)对反应2NO2(g)N2O4(g)△H=-57 2kJ·mol-1①在温度为T1、 T2时,平衡
一定条件下 在体积为10 L的恒容密闭容器中 发生如下反应:2X(s)+Y(g)Z(g) 经60 s
一定条件下,在体积为10 L的恒容密闭容器中,发生如下反应:2X(s)+Y(g)Z(g),经60 s达到平衡,生成0 3 mol Z,下列说法正确的是()A.用X 表示的
在甲 乙两个容积均为1L的密闭容器中 保持两容器的温度相同 进行如下反应:2A(g)+B(g)pC(
在甲、乙两个容积均为1L的密闭容器中,保持两容器的温度相同,进行如下反应:2A(g)+B(g)pC(g),①向甲中通入3molA和1 5molB,达到平衡时测得其中C的体积
已知:N2(g)+3H2(g) 2NH3(g);△H=-Q kJ·mol-1(Q>0)。现有甲乙两
已知:N2(g)+3H2(g) 2NH3(g);△H=-Q kJ·mol-1(Q>0)。现有甲乙两个相同的密闭容器,向甲容器中充入1mol N2(g)和3mol H2(g),在一定条件下达












