半导体生产中常需要控制掺杂 以保证控制电阻率 三氯化磷(PCl3)是一种重要的掺杂剂。实验室要用黄磷
半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)是一种重要的掺杂剂。实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)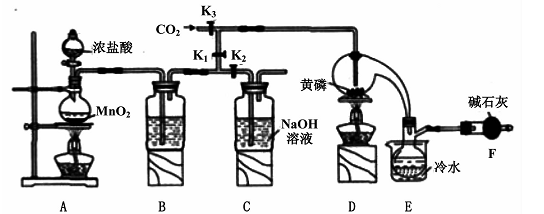 已知黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇水会强烈水解生成H3PO3和HCl;遇O2会生成POCl3,POCl3溶于PCl3。PCl3、POCl3的熔沸点见下表: 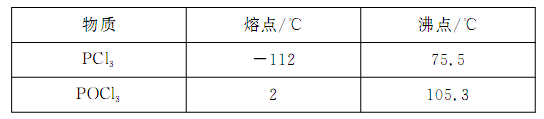 请回答下列问题: (1)A装置中制氯气的离子方程式为 。 (2)B中所装试剂是 ,E中冷水的作用是 ,F中碱石灰的作用是 。 (3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷。通干燥CO2的作用是 。 (4)粗产品中常含有POC13、PCl5等。加入黄磷加热除去PCl5后.通过 (填实验操作名称),即可得到较纯净的PCl3。 (5)通过下面方法可测定产品中PCl3的质量分数 ①迅速称取1.00g产品,加水反应后配成250 mL溶液; ②取以上溶液25.00mL,向其中加入10.00 mL 0.1000 mol/L碘水,充分反应; ③向②所得溶液中加入几滴淀粉溶液,用0.1000 mol/L的Na2S2O3,溶液滴定 ④重复②、③操作,平均消耗Na2S2O3,溶液8.40ml 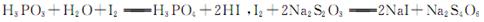 已知: ,假设测定过程中没有其他反应。根据上述数据,该产品中PCl3的质量分数为 。 已知: ,假设测定过程中没有其他反应。根据上述数据,该产品中PCl3的质量分数为 。 |
参考解答
(1)MnO2+4H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O(2)浓H2SO4;冷凝PCl3防止其挥发;吸收多余的氯气,防止空气中的水蒸汽进入烧瓶中和PCl3反应 (3)排尽装置中的空气,防止白磷自燃; (4)蒸馏 (5)79.75% |
试题分析:(1)二氧化锰和浓盐酸加热制取氯气;(2)干燥氯气用浓硫酸;根据表中PCl3的沸点可得,用冷水可以将其冷凝;根据信息可得PCl3不能遇见水蒸气,还要考虑进行尾气处理,故碱石灰的作用为吸收多余的氯气,防止空气中的水蒸汽进入烧瓶中和PCl3反应;(3)根据题目信息可知需要排尽装置内的空气;(4)根据题目信息可知利用沸点的不同将混合物分离,故蒸馏;(5)根据碘单质和Na2S2O3的反应求出剩余的碘单质,根据总的碘单质减去剩余的碘单质求出与H3PO3的物质的量,根据磷原子守恒得PCl3的物质的量,从而求出其质量分数。 |
相似问题
汽车剧烈碰撞时 安全气囊中发生反应10NaN3+2KNO3 = K2O+5Na2O+16N2↑。若氧
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3 = K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是( )A.生成40.0LN2(标
有关氧化还原反应实质的说法中正确的是[ ]A.是否有电子转移 B.是否有元素化合价的变化 C
有关氧化还原反应实质的说法中正确的是[ ]A.是否有电子转移 B.是否有元素化合价的变化 C.是否有氧元素的参加 D.是否有原子的重新组合
将KClO3 I2各0.02 mol加入12 g 36.5%的盐酸中 I2恰好完全溶解 没有气体产生
将KClO3、I2各0 02 mol加入12 g 36 5%的盐酸中,I2恰好完全溶解,没有气体产生(不考虑盐酸的挥发)。将反应后的溶液用冰水冷却,析出橙红色晶体A(A在
(14分)Q W X Y Z是周期表前36号元素中的五种常见元素 其原子序数依次增大。W原子最外层电
(14分)Q、W、X、Y、Z是周期表前36号元素中的五种常见元素,其原子序数依次增大。W原子最外层电子数与核外电子总数之比为3∶4,Q、Y的氧化物是导致酸雨
两种大气污染物NO2和SO2在一定条件下可以发生如下反应:NO2+SO2=' NO' +SO3 在体
两种大气污染物NO2和SO2在一定条件下可以发生如下反应:NO2+SO2=" NO" +SO3,在体积为V L的密闭容器中通入3molNO2和5molSO2, 反应后容器内氮原子和氧












