(14分)某配位化合物为深蓝色晶体 由原子序数依次增大的A B C D E五种元素组成 其原子个数比
| (14分)某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6nsl,回答下列问题。 (1)元素D在周期表中的位置是 。 (2)该配位化合物的化学式为 。 (3)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,两种化合物可任意比互溶,解释其主要原因为 。 (4)A元素与B元素可形成分子式为A2B2的某化合物,该化合物的分子具有平面结构,则其结构式为 。 (5)已知E的晶胞结构如下图所示,又知晶胞边长为3.61×10-8cm,则E的密度为 ;EDC4常作电镀液,其中DC 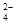 的空间构型是 ,其中D原子的杂化轨道类型是 。 的空间构型是 ,其中D原子的杂化轨道类型是 。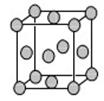 |
参考解答
| (1)三 (1分)ⅥA(1分) (2)Cu(NH3)4SO4·H2O (2分) (3)H2O与H2O2之间形成氢键(2分) (4)H-N=N-H (2分) (5)9.00g·cm-3(2分),正四面体形(2分),sp3杂化(2分) |
试题分析:E元素的外围电子排布为(n-1)dn+6nsl,应用s轨道没有排满,则根据洪特规则可知,此时d轨道应该是全充满状态,即n+6=10,解得n=4,所以E元素的原子序数是18+10+1=29,即E是铜元素。某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1。其中C、D元素同主族且原子序数D为C的二倍,因此符合条件的元素是氧元素与硫元素,即C是O,D是S。根据该配位化合物中原子个数比可知,A应该是氢元素,S与O结合生成硫酸根,剩余1个氧原子与2和氢原子结合形成1分子水,则4个B原子结合12个氢原子,即个数之比为1:3,所以该物质是氨气,即B是氮元素。 (1)硫元素在周期表中的位置是第三周期第ⅥA族。 (2)该配位化合物中氨气是配体,因此化学式为Cu(NH3)4SO4·H2O。 (3)氢元素与氧元素形成的两种常见化合物是水和双氧水,由于氧元素非金属性强,H2O与H2O2之间形成氢键,因此二者互溶。 (4)氢元素与氮元素可形成分子式为A2B2的某化合物是N2H2,该化合物的分子具有平面结构,依据8电子和2电子稳定结构可知,氮元素与氮元素之间形成双键,氢元素与氮元素之间形成单键,则其结构式为H-N=N-H。 (5)根据晶胞结构可知,晶胞中含有铜原子的个数是8× 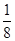 +6× +6× =4,因此 =4,因此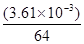 ×6.02×1023=4,解得ρ=9.00g·cm-3。在硫酸根离子中硫原子不存在孤对电子,其价层电子对数是4,所以空间构型是正四面体形,硫原子是sp3杂化。 ×6.02×1023=4,解得ρ=9.00g·cm-3。在硫酸根离子中硫原子不存在孤对电子,其价层电子对数是4,所以空间构型是正四面体形,硫原子是sp3杂化。 |
相似问题
(15分)下表中列出五种短周期元素X Y Z W T的信息。元素相关信息X基态原子最外层电子排布为n
(15分)下表中列出五种短周期元素X、Y、Z、W、T的信息。元素相关信息X基态原子最外层电子排布为nsnnpn+1Y其原子L层电子数是K层3倍Z其单质能与冷水剧烈反
已知原子序数 可推断原子的( )①质子数 ②中子数 ③质量数 ④核电荷
已知原子序数,可推断原子的( )①质子数②中子数③质量数④核电荷数⑤核外电子数⑥原子结构示意图⑦元素在周期表中的位置A.①②③④⑥B.①④⑤⑥⑦C.
下列说法中 正确的是A.第ⅠA族元素都比第ⅡA族元素金属性强B.只含有非金属元素的化合物可能是离子化
下列说法中,正确的是A.第ⅠA族元素都比第ⅡA族元素金属性强B.只含有非金属元素的化合物可能是离子化合物C.只含有共价键的物质一定是共价化合物D.同
(9分)元素周期律是指导我们学习元素及其化合物知识的重要工具。已知氧族元素(不含Po)的部分知识如下
(9分)元素周期律是指导我们学习元素及其化合物知识的重要工具。已知氧族元素(不含Po)的部分知识如下表所示,元素8O16S34Se52Te单质熔点(℃)-218 4113
短周期元素甲 乙 丙 丁的原子序数依次增大 甲和乙形成的气态化合物的水溶液呈碱性 乙位于第VA族 甲
短周期元素甲,乙,丙,丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数和电子层数相等,则 (












